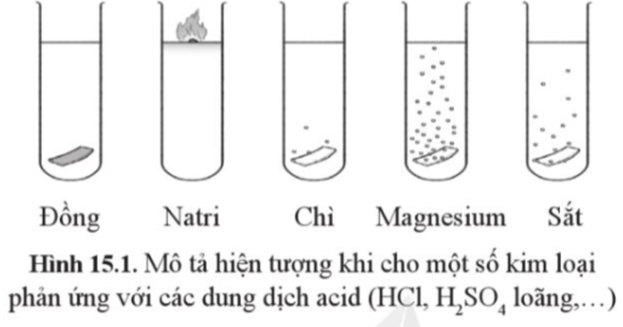
Kim loại phản ứng với dung dịch HCl loãng

Chính Sách Vận Chuyển Và Đổi Trả Hàng
Miễn phí vận chuyển mọi đơn hàng từ 500K
- Phí ship mặc trong nước 50K
- Thời gian nhận hàng 2-3 ngày trong tuần
- Giao hàng hỏa tốc trong 24h
- Hoàn trả hàng trong 30 ngày nếu không hài lòng
Mô tả sản phẩm
Kim loại phản ứng được với dung dịch HCl loãng là những kim loại đứng trước hiđro trong dãy hoạt động hóa học. Điều này có nghĩa là chúng có khả năng đẩy hiđro ra khỏi dung dịch axit và tạo thành muối clorua và khí hiđro.
Danh sách các kim loại phản ứng với HCl loãng
Kim loại phản ứng mạnh:
Những kim loại này phản ứng mạnh với HCl loãng, giải phóng khí hiđro nhanh chóng và mạnh mẽ. Ví dụ bao gồm: Kali (K), Natri (Na), Canxi (Ca), Magie (Mg), Nhôm (Al), Kẽm (Zn), Sắt (Fe).
Kim loại phản ứng yếu hơn:
Một số kim loại phản ứng chậm hơn hoặc cần điều kiện đặc biệt để phản ứng với HCl loãng. Ví dụ như: Thiếc (Sn), Chì (Pb). Lưu ý rằng, một số kim loại như đồng (Cu), bạc (Ag), vàng (Au), bạch kim (Pt) không phản ứng với HCl loãng.
Phương trình phản ứng minh họa
Phản ứng giữa kim loại và HCl loãng thường tạo ra muối clorua và khí hiđro. Ví dụ, phản ứng giữa kẽm và HCl loãng:
Zn + 2HCl → ZnCl2 + H2
Trong phương trình trên, kẽm (Zn) phản ứng với axit clohiđric (HCl) tạo ra muối kẽm clorua (ZnCl2) và khí hiđro (H2).
Các yếu tố ảnh hưởng đến phản ứng
Tốc độ phản ứng của kim loại với HCl loãng phụ thuộc vào một số yếu tố như:
- Độ hoạt động của kim loại: Kim loại càng hoạt động mạnh thì phản ứng càng nhanh.
- Nồng độ HCl: Nồng độ HCl càng cao thì phản ứng càng nhanh.
- Nhiệt độ: Nhiệt độ càng cao thì phản ứng càng nhanh.
- Diện tích tiếp xúc: Diện tích tiếp xúc giữa kim loại và HCl càng lớn thì phản ứng càng nhanh (ví dụ, kim loại dạng bột sẽ phản ứng nhanh hơn kim loại dạng khối).
Xem thêm: các công thức vecto 10
Sản phẩm hữu ích: công thức khoảng cách giữa 2 mặt phẳng
Sản phẩm hữu ích: ăn khoai mì có mập không