Phản ứng giữa Al và H2SO4: Phương trình phản ứng và giải thích

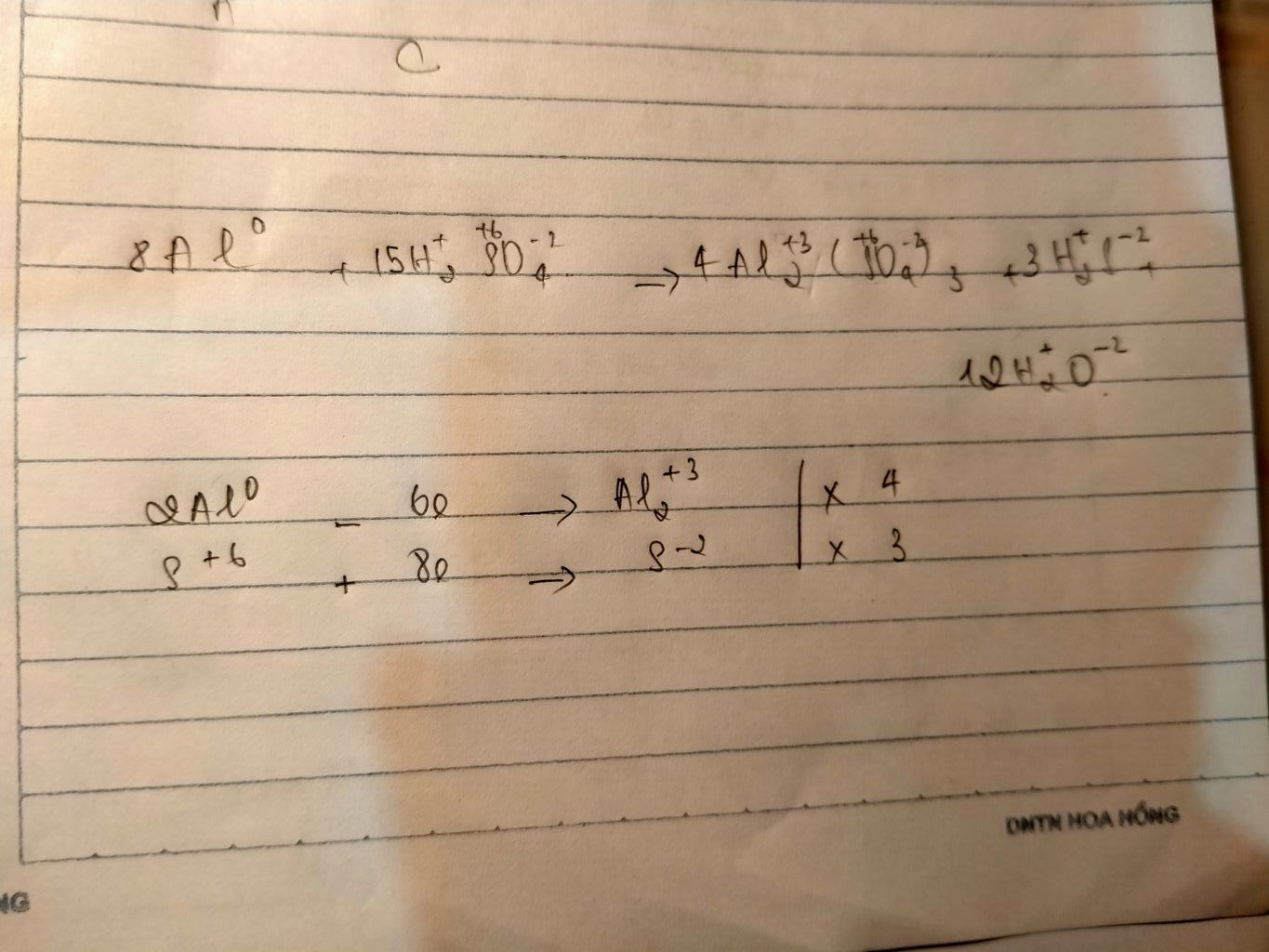

Chính Sách Vận Chuyển Và Đổi Trả Hàng
Miễn phí vận chuyển mọi đơn hàng từ 500K
- Phí ship mặc trong nước 50K
- Thời gian nhận hàng 2-3 ngày trong tuần
- Giao hàng hỏa tốc trong 24h
- Hoàn trả hàng trong 30 ngày nếu không hài lòng
Mô tả sản phẩm
Phản ứng giữa nhôm (Al) và axit sunfuric (H2SO4) không tạo ra sản phẩm là Al2(SO4)3, H2S và H2O như phương trình bạn đưa ra. Phương trình đó là không chính xác về mặt hóa học. Nhôm phản ứng với axit sunfuric loãng tạo ra muối nhôm sunfat và khí hydro.
Phương trình phản ứng chính xác
Nhôm phản ứng với axit sunfuric loãng:
Phương trình phản ứng cân bằng chính xác là: 2Al + 3H2SO4 → Al2(SO4)3 + 3H2 Trong phản ứng này, nhôm bị oxi hóa từ số oxi hóa 0 lên +3, trong khi ion H+ trong axit sunfuric bị khử xuống 0 tạo thành khí hydro (H2). Axit sunfuric đóng vai trò là chất oxi hóa. Sản phẩm tạo thành là muối nhôm sunfat (Al2(SO4)3) và khí hydro (H2).Nhôm phản ứng với axit sunfuric đặc, nóng:
Khi phản ứng với axit sunfuric đặc, nóng, phản ứng sẽ phức tạp hơn và có thể tạo ra sản phẩm khác. Tuy nhiên, H2S không phải là sản phẩm chính trong trường hợp này. Sản phẩm chính thường là muối nhôm sunfat, nước và khí lưu huỳnh đioxit (SO2). Phương trình phản ứng sẽ phức tạp hơn và cần phải cân bằng kỹ lưỡng dựa trên điều kiện phản ứng cụ thể. Việc hiểu rõ điều kiện phản ứng (nồng độ axit, nhiệt độ) là rất quan trọng để xác định chính xác sản phẩm tạo thành. Phương trình phản ứng bạn đề cập ban đầu là sai và không phản ánh đúng quá trình hóa học xảy ra. Hãy luôn đảm bảo sử dụng phương trình phản ứng cân bằng và chính xác để tránh hiểu lầm.Xem thêm: bảng tóm tắt 12 thì trong tiếng anh
Xem thêm: các công thức toán 9 thi vào lớp 10
Sản phẩm liên quan: bảng đơn vị đo ml
Sản phẩm liên quan: em học giỏi tiếng anh lớp 3