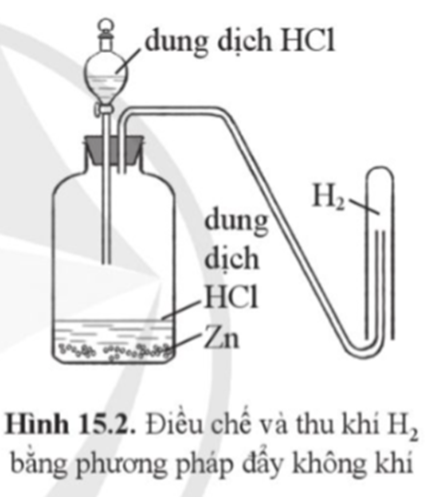
Xét phản ứng điều chế H2 trong phòng thí nghiệm

Chính Sách Vận Chuyển Và Đổi Trả Hàng
Miễn phí vận chuyển mọi đơn hàng từ 500K
- Phí ship mặc trong nước 50K
- Thời gian nhận hàng 2-3 ngày trong tuần
- Giao hàng hỏa tốc trong 24h
- Hoàn trả hàng trong 30 ngày nếu không hài lòng
Mô tả sản phẩm
Để điều chế khí hiđro (H2) trong phòng thí nghiệm, người ta thường sử dụng phản ứng giữa các kim loại hoạt động với các axit loãng. Đây là phương pháp phổ biến và tương đối an toàn. Bài viết này sẽ đi sâu vào xét phản ứng điều chế H2 trong phòng thí nghiệm, bao gồm các phương pháp, hiện tượng quan sát được và những lưu ý quan trọng.
Các phương pháp điều chế H2 trong phòng thí nghiệm
Phương pháp sử dụng kim loại và axit
Đây là phương pháp phổ biến nhất. Kim loại hoạt động như Zn, Fe, Mg, Al phản ứng với axit như HCl hoặc H2SO4 loãng tạo ra khí H2 và muối tương ứng. Ví dụ: Zn + 2HCl → ZnCl2 + H2↑ Phản ứng này diễn ra khá nhanh và dễ quan sát hiện tượng sủi bọt khí. Tuy nhiên, cần lựa chọn kim loại và axit phù hợp để đảm bảo phản ứng xảy ra hiệu quả và an toàn.Phương pháp điện phân nước
Phương pháp này sử dụng dòng điện để phân hủy nước thành H2 và O2. Đây là phương pháp sạch hơn nhưng yêu cầu thiết bị chuyên dụng và điều kiện thực hiện phức tạp hơn. Phản ứng điện phân nước: 2H2O → 2H2↑ + O2↑Hiện tượng quan sát được trong phản ứng điều chế H2
Khi cho kim loại phản ứng với axit, ta quan sát thấy hiện tượng sủi bọt khí không màu, không mùi. Khí này chính là H2. Đồng thời, dung dịch phản ứng có thể thay đổi màu sắc hoặc nhiệt độ tùy thuộc vào loại kim loại và axit được sử dụng.Lưu ý an toàn khi điều chế H2 trong phòng thí nghiệm
Khí H2 rất dễ cháy và nổ khi trộn lẫn với không khí. Vì vậy, cần thực hiện thí nghiệm trong phòng thông thoáng, tránh xa nguồn lửa và các thiết bị phát nhiệt. Cần tuân thủ các quy tắc an toàn trong phòng thí nghiệm và sử dụng các thiết bị bảo hộ cá nhân như kính bảo hộ, găng tay… Ngoài ra, cần chú ý đến việc xử lý chất thải sau khi thí nghiệm.Sản phẩm hữu ích: u chia v tất cả đạo hàm
Xem thêm: cách sửa khoảng trống trong word