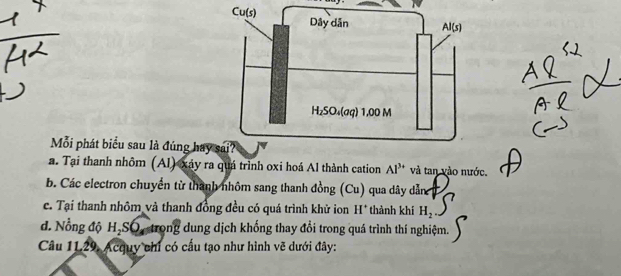
Quá trình tạo thành ion Al3+ nào sau đây là đúng?
Chính Sách Vận Chuyển Và Đổi Trả Hàng
Miễn phí vận chuyển mọi đơn hàng từ 500K
- Phí ship mặc trong nước 50K
- Thời gian nhận hàng 2-3 ngày trong tuần
- Giao hàng hỏa tốc trong 24h
- Hoàn trả hàng trong 30 ngày nếu không hài lòng
Mô tả sản phẩm
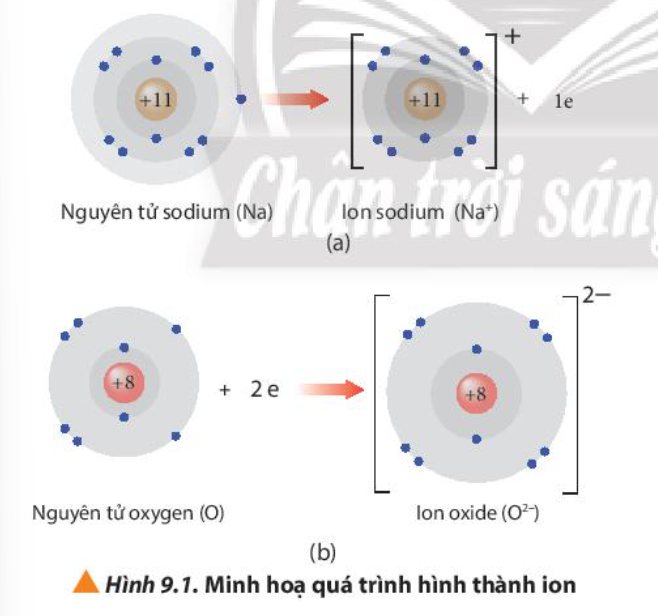
Quá trình tạo thành ion Al3+ đúng là: Nguyên tử nhôm (Al) mất 3 electron ở lớp ngoài cùng để đạt cấu hình electron bền vững của khí hiếm Neon (Ne).
Hiểu về cấu tạo nguyên tử Nhôm
Cấu hình electron của nguyên tử Nhôm
Nguyên tử Nhôm (Al) có số hiệu nguyên tử là 13, có cấu hình electron là 1s²2s²2p⁶3s²3p¹. Lớp electron ngoài cùng của Al có 3 electron. Để đạt được cấu hình electron bền vững, giống như khí hiếm Neon (Ne) (1s²2s²2p⁶), nguyên tử Al có xu hướng nhường đi 3 electron này.Quá trình hình thành ion Al3+
Sự mất electron và sự tạo thành ion
Khi nguyên tử Al mất đi 3 electron ở lớp ngoài cùng, nó trở thành ion Al3+ mang điện tích dương. Quá trình này được biểu diễn bằng phương trình: Al → Al³⁺ + 3e⁻Tại sao Al nhường 3 electron?
Việc nhường 3 electron giúp Al đạt được cấu hình electron bền vững của khí hiếm Neon (Ne), có 8 electron ở lớp ngoài cùng (octet). Cấu hình electron bền vững giúp nguyên tử trở nên ổn định hơn về mặt năng lượng. Đây là nguyên lý cơ bản chi phối sự hình thành ion trong hóa học.Các quá trình sai
Một số quá trình khác có thể được đưa ra nhưng không đúng vì chúng không tuân theo nguyên tắc đạt được cấu hình electron bền vững. Ví dụ, Al không thể nhận thêm electron để đạt cấu hình bền vững vì việc này sẽ làm cho lớp electron ngoài cùng trở nên quá đầy.Sản phẩm hữu ích: đồng nghĩa với vui vẻ
Xem thêm: down round là gì
Sản phẩm hữu ích: status về sự cố gắng
Sản phẩm liên quan: vàng tên hoá học