Phản ứng đốt cháy Ethanol: Phương trình, sản phẩm và ứng dụng

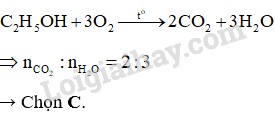

Chính Sách Vận Chuyển Và Đổi Trả Hàng
Miễn phí vận chuyển mọi đơn hàng từ 500K
- Phí ship mặc trong nước 50K
- Thời gian nhận hàng 2-3 ngày trong tuần
- Giao hàng hỏa tốc trong 24h
- Hoàn trả hàng trong 30 ngày nếu không hài lòng
Mô tả sản phẩm
Phản ứng đốt cháy ethanol là phản ứng giữa ethanol (C₂H₅OH) với oxy (O₂) tạo ra khí cacbonic (CO₂), hơi nước (H₂O) và năng lượng dưới dạng nhiệt. Đây là một phản ứng oxy hóa hoàn toàn, giải phóng một lượng nhiệt đáng kể.
Phương trình phản ứng đốt cháy Ethanol
Phương trình hóa học cân bằng cho phản ứng đốt cháy hoàn toàn ethanol là:
C₂H₅OH(l) + 3O₂(g) → 2CO₂(g) + 3H₂O(g)
Trong đó:
- C₂H₅OH(l): Ethanol ở thể lỏng
- O₂(g): Oxy ở thể khí
- CO₂(g): Cacbon đioxit ở thể khí
- H₂O(g): Nước ở thể khí
Phản ứng này tỏa nhiệt, nghĩa là nó giải phóng năng lượng ra môi trường xung quanh. Lượng nhiệt tỏa ra này phụ thuộc vào lượng ethanol được đốt cháy.
Sản phẩm của phản ứng đốt cháy Ethanol
Như phương trình phản ứng đã chỉ ra, sản phẩm chính của phản ứng đốt cháy ethanol là cacbon đioxit (CO₂) và nước (H₂O). Cả hai đều là chất khí ở nhiệt độ cao của phản ứng. Cacbon đioxit là một khí nhà kính, góp phần vào hiệu ứng nhà kính. Nước, mặc dù không độc hại, nhưng nếu ở dạng hơi với nồng độ cao cũng có thể gây khó thở.
Ứng dụng của phản ứng đốt cháy Ethanol
Phản ứng đốt cháy ethanol có nhiều ứng dụng quan trọng trong thực tế, bao gồm:
Sản xuất năng lượng:
Ethanol là một nhiên liệu sinh học tiềm năng, được sử dụng trong các động cơ đốt trong. Việc đốt cháy ethanol tạo ra năng lượng để vận hành các phương tiện giao thông, máy móc…
Nhiệt:
Nhiệt tỏa ra từ phản ứng đốt cháy ethanol có thể được sử dụng để sưởi ấm hoặc nấu ăn. Tuy nhiên, ứng dụng này ít phổ biến hơn so với việc sử dụng ethanol làm nhiên liệu.
Ứng dụng trong phòng thí nghiệm:
Trong phòng thí nghiệm, phản ứng đốt cháy ethanol có thể được sử dụng để xác định một số thông số liên quan đến nhiệt động lực học của phản ứng.
Tuy nhiên, cần lưu ý rằng việc đốt cháy ethanol cần được thực hiện một cách an toàn, tránh nguy cơ cháy nổ và ngộ độc khí.
Xem thêm: kmno4 + nacl + h2so4
Xem thêm: glucozo tác dụng với agno3
Xem thêm: bao lực học đường hậu quả
Sản phẩm liên quan: dạng bài toán đổi đơn vị lớp 4