Oxi hóa khử là gì?
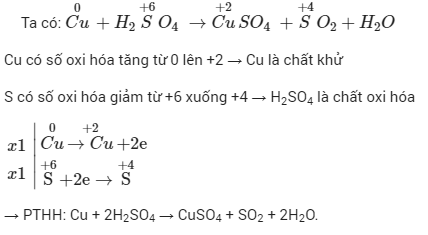
Chính Sách Vận Chuyển Và Đổi Trả Hàng
Miễn phí vận chuyển mọi đơn hàng từ 500K
- Phí ship mặc trong nước 50K
- Thời gian nhận hàng 2-3 ngày trong tuần
- Giao hàng hỏa tốc trong 24h
- Hoàn trả hàng trong 30 ngày nếu không hài lòng
Mô tả sản phẩm
Oxi hóa khử là phản ứng hóa học xảy ra sự trao đổi electron giữa các chất, cụ thể là sự tăng và giảm số oxi hóa của các nguyên tố. Trong phản ứng này, một chất nhường electron (bị oxi hóa) và một chất nhận electron (bị khử).
Quá trình oxi hóa và khử
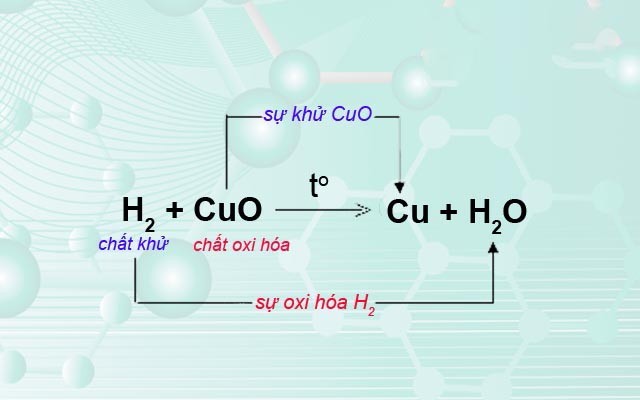
Sự oxi hóa
Sự oxi hóa là quá trình một chất mất electron, dẫn đến tăng số oxi hóa. Ví dụ: khi sắt bị oxi hóa thành sắt (III) oxit (Fe₂O₃), nguyên tử sắt mất electron và số oxi hóa của sắt tăng từ 0 lên +3.Sự khử
Sự khử là quá trình một chất nhận electron, dẫn đến giảm số oxi hóa. Ví dụ: trong phản ứng trên, oxy nhận electron từ sắt và số oxi hóa của oxy giảm từ 0 xuống -2.Đặc điểm của phản ứng oxi hóa khử
Phản ứng oxi hóa khử luôn xảy ra đồng thời, nghĩa là sự oxi hóa của một chất luôn kèm theo sự khử của một chất khác. Số electron mất đi trong quá trình oxi hóa bằng số electron nhận được trong quá trình khử. Đây là nguyên tắc bảo toàn điện tích.Ứng dụng của phản ứng oxi hóa khử
Phản ứng oxi hóa khử có vai trò quan trọng trong nhiều lĩnh vực, bao gồm:Công nghiệp
Sản xuất kim loại từ quặng, sản xuất pin, ắc quy, công nghệ xử lý nước thải...Sinh học
Hô hấp tế bào, quang hợp, quá trình chuyển hóa năng lượng trong cơ thể sống...Ví dụ về phản ứng oxi hóa khử
Phản ứng giữa Zn và HCl là một ví dụ điển hình: Zn + 2HCl → ZnCl₂ + H₂. Trong phản ứng này, Zn bị oxi hóa (mất electron) và H+ bị khử (nhận electron). Tóm lại, hiểu rõ về oxi hóa khử là rất quan trọng để nắm vững nhiều khía cạnh của hóa học và các ứng dụng thực tiễn của nó.Xem thêm: canh chua rau nhút
Sản phẩm hữu ích: hình xăm chữ family
Xem thêm: hái hoa rừng cho em