Nhiệt Phân Kali Clorat
Chính Sách Vận Chuyển Và Đổi Trả Hàng
Miễn phí vận chuyển mọi đơn hàng từ 500K
- Phí ship mặc trong nước 50K
- Thời gian nhận hàng 2-3 ngày trong tuần
- Giao hàng hỏa tốc trong 24h
- Hoàn trả hàng trong 30 ngày nếu không hài lòng
Mô tả sản phẩm
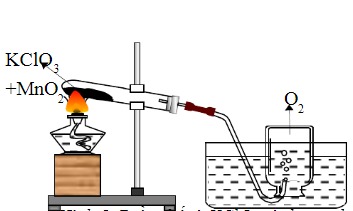
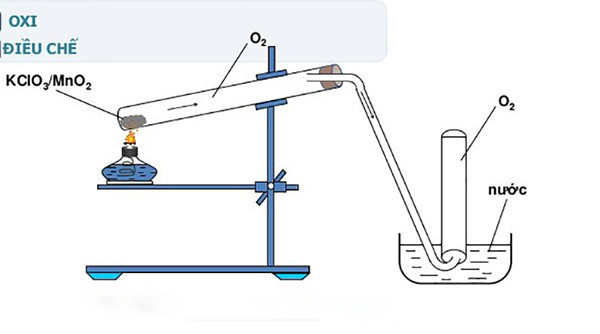
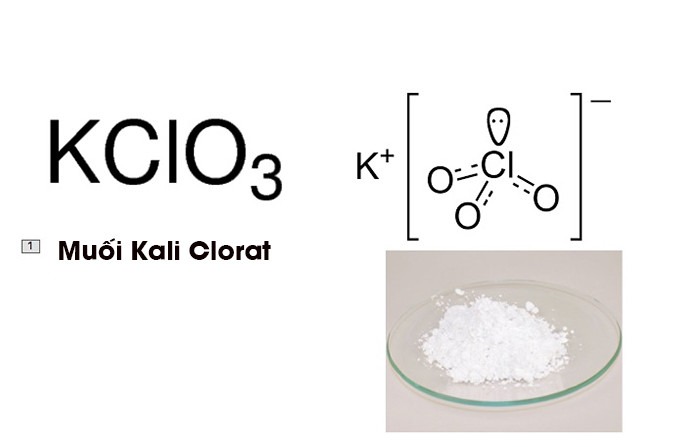
Nhiệt phân kali clorat (KClO3) là quá trình phân hủy muối này thành kali clorua (KCl) và khí oxi (O2) khi được đun nóng. Đây là một phản ứng oxi hóa khử quan trọng, được sử dụng rộng rãi trong phòng thí nghiệm để sản xuất khí oxi.
Phản ứng nhiệt phân kali clorat
Phương trình phản ứng:
2KClO3(s) → 2KCl(s) + 3O2(g)
Như bạn thấy, hai phân tử kali clorat sẽ tạo ra hai phân tử kali clorua và ba phân tử khí oxi. Phản ứng này cần được xúc tác bởi một chất xúc tác, thường là mangan đioxit (MnO2), để xảy ra ở nhiệt độ thấp hơn và nhanh hơn. Mangan đioxit không bị thay đổi trong quá trình phản ứng.
Điều kiện phản ứng:
Phản ứng nhiệt phân kali clorat cần được thực hiện ở nhiệt độ cao, thường trên 368°C. Việc sử dụng chất xúc tác như mangan đioxit (MnO2) giúp làm giảm nhiệt độ cần thiết cho phản ứng và tăng tốc độ phản ứng. Phản ứng này giải phóng một lượng nhiệt đáng kể.
Ứng dụng của phản ứng nhiệt phân kali clorat
Sản xuất khí oxi:
Đây là ứng dụng chính của phản ứng này trong phòng thí nghiệm. Khí oxi thu được có độ tinh khiết cao và có thể được sử dụng trong nhiều thí nghiệm khác nhau.
Ứng dụng khác:
Ngoài việc sản xuất khí oxi, kali clorat còn được sử dụng trong một số ứng dụng khác như trong sản xuất pháo hoa, thuốc nổ và một số chất tẩy trắng.
An toàn khi tiến hành thí nghiệm
Khi tiến hành thí nghiệm nhiệt phân kali clorat, cần phải tuân thủ các biện pháp an toàn để tránh tai nạn. Cần đeo kính bảo hộ và găng tay để bảo vệ mắt và da. Thí nghiệm nên được thực hiện trong tủ hút để tránh hít phải khí độc hại. Không được đun nóng kali clorat quá mạnh hoặc quá nhanh để tránh gây nổ.
Xem thêm: toán giải lớp 3
Sản phẩm hữu ích: tách rời hay tách dời
Xem thêm: k2cr2o7 + ki + h2so4
Xem thêm: bài thơ tặng cháu