Phương trình ion rút gọn NH4Cl + KOH

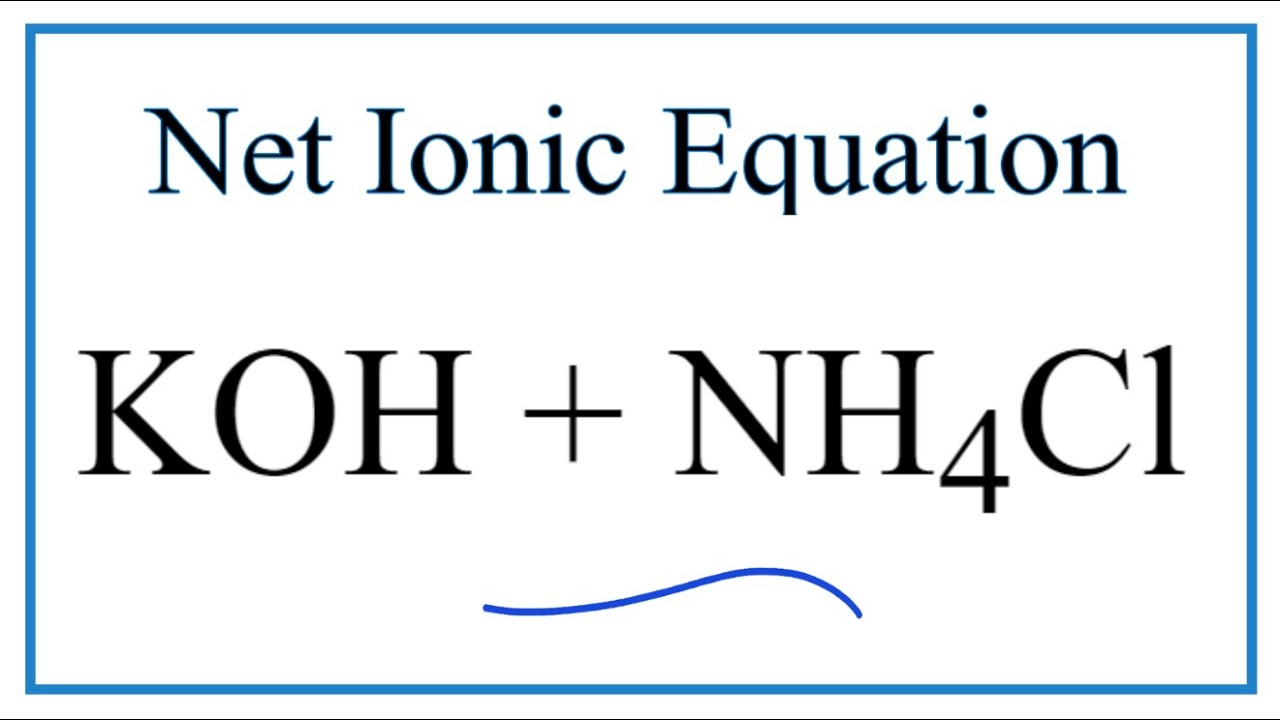

Chính Sách Vận Chuyển Và Đổi Trả Hàng
Miễn phí vận chuyển mọi đơn hàng từ 500K
- Phí ship mặc trong nước 50K
- Thời gian nhận hàng 2-3 ngày trong tuần
- Giao hàng hỏa tốc trong 24h
- Hoàn trả hàng trong 30 ngày nếu không hài lòng
Mô tả sản phẩm
Phản ứng giữa NH4Cl và KOH tạo ra khí amoniac (NH3), nước (H2O) và muối KCl. Phương trình ion rút gọn của phản ứng này là: NH4+ + OH- → NH3 + H2O
Hiểu rõ phản ứng giữa NH4Cl và KOH
Các chất tham gia phản ứng
NH4Cl (Amoni clorua) là một muối tạo bởi bazơ yếu NH3 và axit mạnh HCl. KOH (Kali hydroxit) là một bazơ mạnh. Khi hai chất này tác dụng với nhau, phản ứng trung hòa xảy ra.
Phương trình phản ứng đầy đủ
Phương trình phản ứng đầy đủ là: NH4Cl(dd) + KOH(dd) → KCl(dd) + NH3(k) + H2O(l)
Viết phương trình ion
Để viết phương trình ion đầy đủ, ta cần phân ly các chất điện ly mạnh thành ion: NH4+ + Cl- + K+ + OH- → K+ + Cl- + NH3 + H2O
Phương trình ion rút gọn
Trong phương trình ion đầy đủ, ion K+ và Cl- là ion ngoài môi trường, không tham gia phản ứng. Do đó, phương trình ion rút gọn là: NH4+ + OH- → NH3 + H2O
Ứng dụng thực tế
Phản ứng này được ứng dụng trong một số thí nghiệm hóa học để nhận biết ion amoni (NH4+) hoặc để điều chế khí amoniac trong phòng thí nghiệm. Mùi khai đặc trưng của NH3 là dấu hiệu nhận biết rõ ràng cho phản ứng này.
Sản phẩm liên quan: khái niệm chất béo
Xem thêm: mệnh lệnh thôi miên
Sản phẩm liên quan: 3 anh trai của tôi
Xem thêm: c2h5oh ra axit axetic
Sản phẩm liên quan: đổi dấu chấm thành dấu phẩy