Các Yếu Tố Ảnh Hưởng Đến Cân Bằng Hóa Học

Chính Sách Vận Chuyển Và Đổi Trả Hàng
Miễn phí vận chuyển mọi đơn hàng từ 500K
- Phí ship mặc trong nước 50K
- Thời gian nhận hàng 2-3 ngày trong tuần
- Giao hàng hỏa tốc trong 24h
- Hoàn trả hàng trong 30 ngày nếu không hài lòng
Mô tả sản phẩm
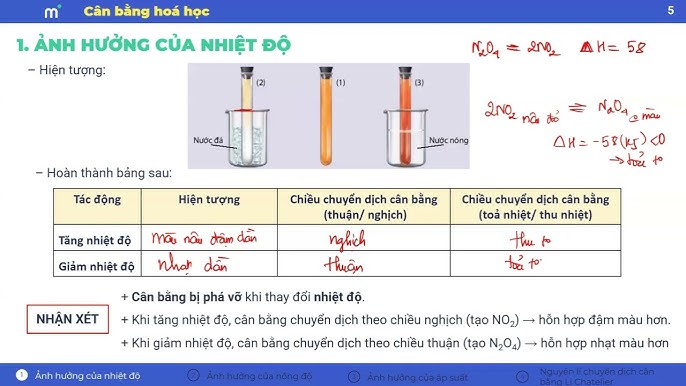
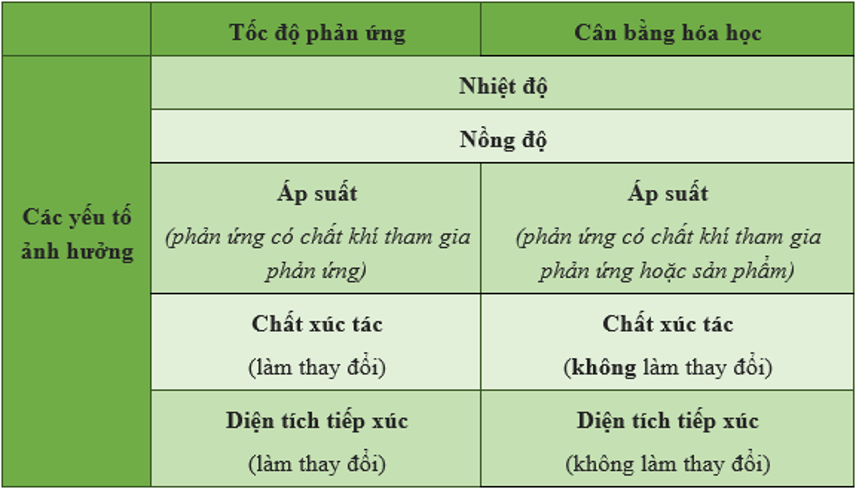
Các yếu tố ảnh hưởng đến cân bằng hóa học bao gồm sự thay đổi nồng độ chất phản ứng và sản phẩm, thay đổi nhiệt độ, thay đổi áp suất (đối với phản ứng có khí tham gia) và sự có mặt của chất xúc tác. Hiểu rõ các yếu tố này giúp dự đoán và điều khiển hướng dịch chuyển cân bằng, tối ưu hóa hiệu suất phản ứng.
1. Thay Đổi Nồng Độ
1.1 Tăng Nồng Độ Chất Phản Ứng:
Cân bằng sẽ dịch chuyển về phía sản phẩm, làm tăng lượng sản phẩm hình thành.1.2 Giảm Nồng Độ Chất Phản Ứng:
Cân bằng sẽ dịch chuyển về phía chất phản ứng, làm giảm lượng sản phẩm.1.3 Tăng Nồng Độ Sản Phẩm:
Cân bằng sẽ dịch chuyển về phía chất phản ứng, làm giảm lượng sản phẩm.1.4 Giảm Nồng Độ Sản Phẩm:
Cân bằng sẽ dịch chuyển về phía sản phẩm, làm tăng lượng sản phẩm hình thành.2. Thay Đổi Nhiệt Độ
2.1 Phản Ứng Thu Nhiệt (ΔH > 0):
Tăng nhiệt độ sẽ làm cân bằng dịch chuyển về phía sản phẩm. Giảm nhiệt độ sẽ làm cân bằng dịch chuyển về phía chất phản ứng.2.2 Phản Ứng Tỏa Nhiệt (ΔH < 0):
Tăng nhiệt độ sẽ làm cân bằng dịch chuyển về phía chất phản ứng. Giảm nhiệt độ sẽ làm cân bằng dịch chuyển về phía sản phẩm.3. Thay Đổi Áp Suất
3.1 Ảnh hưởng của áp suất:
Áp suất chỉ ảnh hưởng đến cân bằng của các phản ứng có sự tham gia của chất khí. Tăng áp suất sẽ làm cân bằng dịch chuyển về phía số mol khí nhỏ hơn. Giảm áp suất sẽ làm cân bằng dịch chuyển về phía số mol khí lớn hơn.4. Chất Xúc Tác
4.1 Vai trò của chất xúc tác:
Chất xúc tác làm tăng tốc độ phản ứng thuận và nghịch như nhau, do đó không làm thay đổi vị trí cân bằng mà chỉ làm cho cân bằng đạt được nhanh hơn.Xem thêm: khái niệm liên kết cộng hóa trị
Sản phẩm hữu ích: base là gì hóa
Xem thêm: dàn ý về lòng nhân ái
Sản phẩm liên quan: nghe - viết chính tả lớp 2 cánh diều
Sản phẩm hữu ích: tất cả các ký hiệu điện