Phản ứng Al + HCl: Hiện tượng và Giải thích


Chính Sách Vận Chuyển Và Đổi Trả Hàng
Miễn phí vận chuyển mọi đơn hàng từ 500K
- Phí ship mặc trong nước 50K
- Thời gian nhận hàng 2-3 ngày trong tuần
- Giao hàng hỏa tốc trong 24h
- Hoàn trả hàng trong 30 ngày nếu không hài lòng
Mô tả sản phẩm
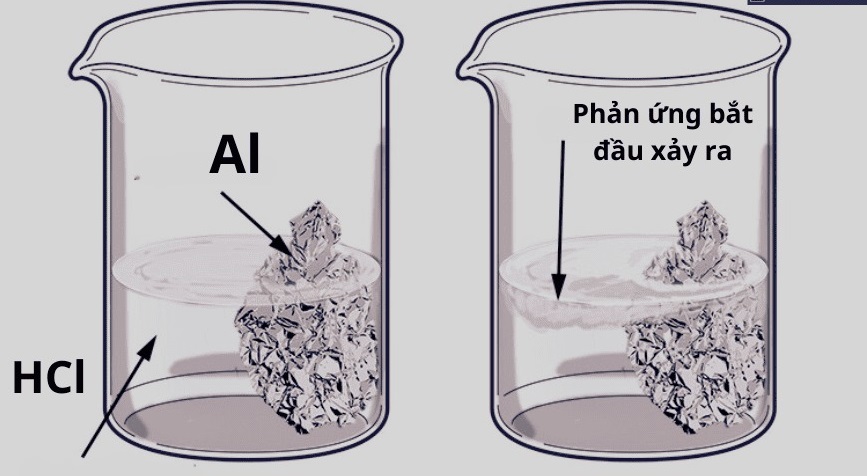
Khi cho nhôm (Al) phản ứng với axit clohiđric (HCl), hiện tượng quan sát được là nhôm tan dần trong dung dịch axit, đồng thời có khí không màu, không mùi thoát ra, đó là khí hiđro (H2). Dung dịch thu được có màu trong suốt.
Phản ứng hóa học
Phương trình phản ứng:
2Al + 6HCl → 2AlCl3 + 3H2
Giải thích hiện tượng:
Nhôm là kim loại hoạt động hóa học mạnh, nó phản ứng với axit clohiđric tạo thành muối nhôm clorua (AlCl3) và giải phóng khí hiđro. Khí hiđro thoát ra chính là nguyên nhân gây ra hiện tượng sủi bọt khí mà bạn quan sát được. Quá trình phản ứng diễn ra mạnh mẽ hay yếu ớt phụ thuộc vào nồng độ của axit HCl và diện tích tiếp xúc của nhôm. Việc nhôm tan dần là do nhôm bị oxi hóa và chuyển thành ion Al3+ trong dung dịch.
Các yếu tố ảnh hưởng đến phản ứng
Nồng độ axit:
Nồng độ axit HCl càng cao thì phản ứng diễn ra càng nhanh và mạnh mẽ. Với dung dịch HCl loãng, phản ứng sẽ diễn ra chậm hơn.
Diện tích tiếp xúc:
Nếu nhôm được nghiền thành bột thì diện tích tiếp xúc giữa nhôm và axit sẽ tăng lên, làm cho phản ứng diễn ra nhanh hơn. Ngược lại, nếu dùng nhôm dạng khối lớn, phản ứng sẽ diễn ra chậm hơn.
Nhiệt độ:
Tăng nhiệt độ sẽ làm tăng tốc độ phản ứng. Tuy nhiên, cần lưu ý an toàn khi thực hiện thí nghiệm ở nhiệt độ cao.
Ứng dụng
Phản ứng giữa nhôm và axit clohiđric được ứng dụng trong nhiều lĩnh vực, chẳng hạn như sản xuất hiđro trong công nghiệp, tổng hợp các hợp chất nhôm khác, và trong một số ứng dụng khác trong hóa học.
Xem thêm: đề toán lớp 3
Xem thêm: c5h12o có bao nhiêu ancol bậc 2
Sản phẩm liên quan: c6h12o6 cu oh 2