1s2 2s2 2p6 3s2 3p6 là cấu hình electron của nguyên tố Argon (Ar), một khí hiếm nằm ở chu kì 3, nhóm VIIIA trong bảng tuần hoàn.
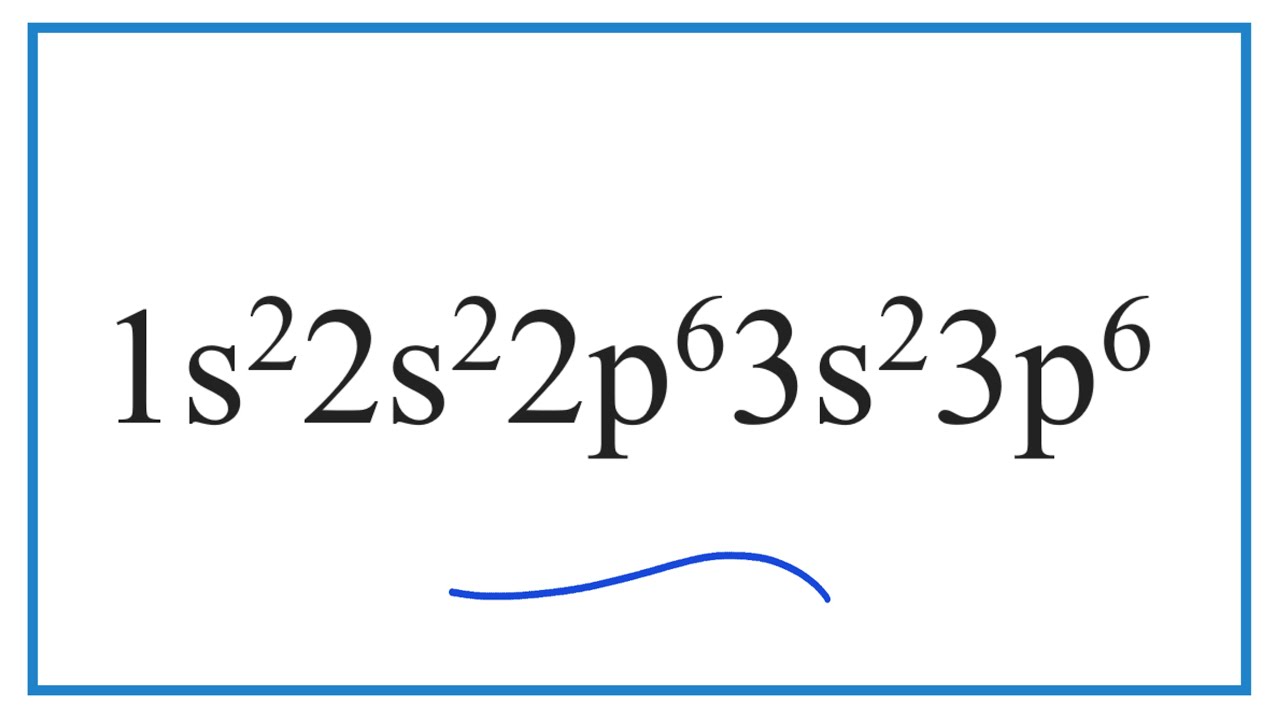

Chính Sách Vận Chuyển Và Đổi Trả Hàng
Miễn phí vận chuyển mọi đơn hàng từ 500K
- Phí ship mặc trong nước 50K
- Thời gian nhận hàng 2-3 ngày trong tuần
- Giao hàng hỏa tốc trong 24h
- Hoàn trả hàng trong 30 ngày nếu không hài lòng
Mô tả sản phẩm
1s2 2s2 2p6 3s2 3p6 là cấu hình electron của nguyên tử Argon (Ar), một khí hiếm. Cấu hình này cho thấy Argon có tổng cộng 18 electron, được phân bố trên các lớp electron như sau: lớp K (n=1) có 2 electron, lớp L (n=2) có 8 electron và lớp M (n=3) có 8 electron. Việc lớp electron ngoài cùng (lớp M) đã bão hòa với 8 electron giải thích tại sao Argon là một khí hiếm, có tính chất hóa học rất trơ.
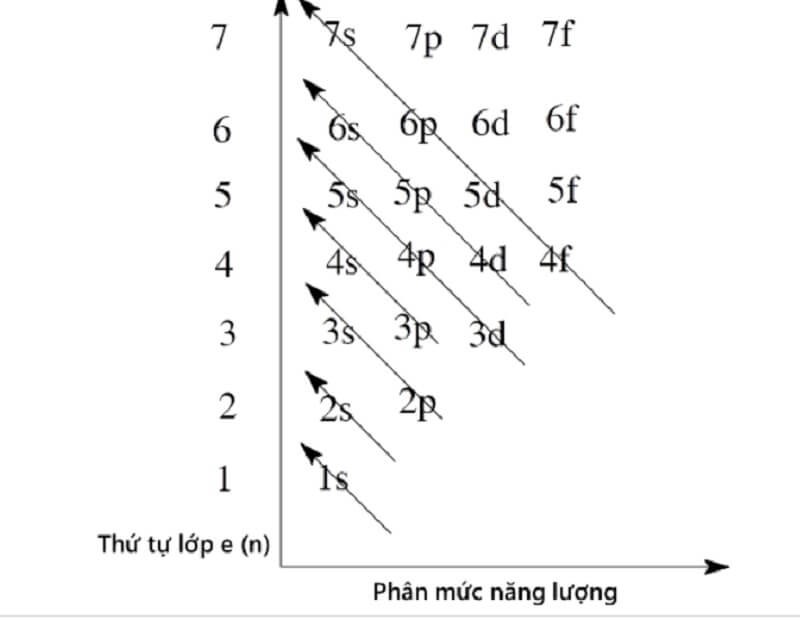
Phân tích cấu hình electron 1s2 2s2 2p6 3s2 3p6
Lớp electron và số electron
Mỗi số trong cấu hình electron đại diện cho một lớp electron. Số mũ trên mỗi ký hiệu orbital (s, p, d, f) cho biết số electron trong orbital đó. Ví dụ, 1s2 có nghĩa là lớp electron đầu tiên (n=1) có 2 electron trong orbital s. Tổng số electron trong cấu hình này là 18, tương ứng với số nguyên tử của Argon.Tính chất hóa học của Argon
Do lớp electron ngoài cùng đã bão hòa với 8 electron (octet), Argon có xu hướng không tham gia vào các phản ứng hóa học. Điều này làm cho Argon trở thành một khí hiếm, rất trơ và ít phản ứng với các chất khác. Tính chất này của Argon được ứng dụng rộng rãi trong nhiều lĩnh vực như hàn, bảo quản thực phẩm, và làm chất khí trơ trong các bóng đèn.Ứng dụng của Argon
Tính chất trơ của Argon khiến nó trở thành một chất khí quan trọng trong nhiều ứng dụng công nghiệp. Một số ứng dụng đáng chú ý bao gồm:- Hàn hồ quang
- Sản xuất kim loại
- Bảo quản thực phẩm
- Chiếu sáng
- Thiết bị y tế
Sản phẩm hữu ích: các công thức tính nhanh toán 12
Sản phẩm liên quan: uong nuoc la tia to co tot ko
Xem thêm: nguyệt thực là hiện tượng gì