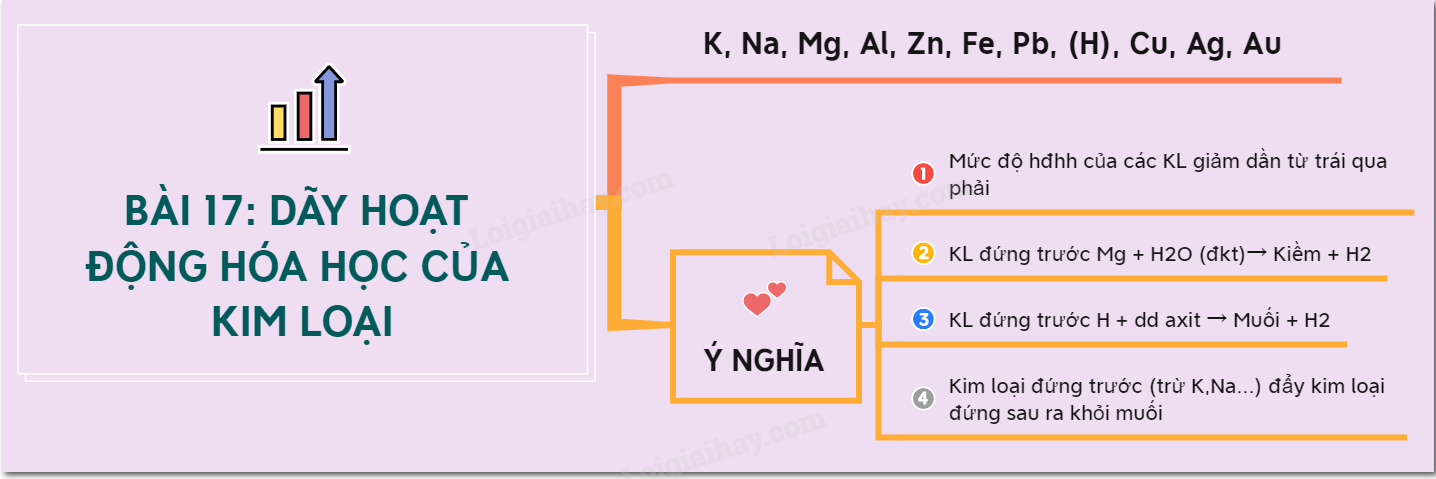
Ý nghĩa của dãy hoạt động hóa học


Chính Sách Vận Chuyển Và Đổi Trả Hàng
Miễn phí vận chuyển mọi đơn hàng từ 500K
- Phí ship mặc trong nước 50K
- Thời gian nhận hàng 2-3 ngày trong tuần
- Giao hàng hỏa tốc trong 24h
- Hoàn trả hàng trong 30 ngày nếu không hài lòng
Mô tả sản phẩm
Dãy hoạt động hóa học cho biết khả năng hoạt động hóa học của các kim loại, giúp chúng ta dự đoán được phản ứng giữa kim loại với các chất khác như dung dịch axit, muối… Tóm lại, dãy hoạt động hóa học là công cụ quan trọng trong hóa học để dự đoán và hiểu được các phản ứng hóa học.
Ứng dụng của dãy hoạt động hóa học
Dự đoán phản ứng giữa kim loại và dung dịch axit
Kim loại đứng trước hiđro trong dãy hoạt động hóa học sẽ phản ứng với dung dịch axit (HCl, H2SO4 loãng) giải phóng khí hiđro. Ví dụ: Zn + 2HCl → ZnCl2 + H2. Kim loại đứng sau hiđro sẽ không phản ứng với axit loãng.
Dự đoán phản ứng giữa kim loại và dung dịch muối
Kim loại hoạt động mạnh hơn sẽ đẩy kim loại hoạt động yếu hơn ra khỏi dung dịch muối của nó. Ví dụ: Fe + CuSO4 → FeSO4 + Cu. Kim loại đứng trước sẽ đẩy kim loại đứng sau ra khỏi dung dịch muối của nó.
Ứng dụng trong luyện kim
Dãy hoạt động hóa học giúp lựa chọn phương pháp thích hợp để điều chế kim loại. Kim loại đứng sau trong dãy hoạt động hóa học thường được điều chế bằng phương pháp điện phân, còn kim loại đứng trước có thể được điều chế bằng phương pháp khác như khử oxit kim loại bằng các chất khử như Cacbon, Hiđro,...
Cấu tạo và cách sử dụng dãy hoạt động hóa học
Cấu tạo
Dãy hoạt động hóa học được sắp xếp theo thứ tự giảm dần khả năng hoạt động hóa học của kim loại. Kim loại đứng trước có khả năng hoạt động hóa học mạnh hơn kim loại đứng sau.
Cách sử dụng
Để sử dụng dãy hoạt động hóa học, ta cần xác định vị trí của kim loại trong dãy. Kim loại đứng trước sẽ phản ứng mạnh hơn với các chất khác so với kim loại đứng sau. Việc so sánh vị trí của kim loại trong dãy hoạt động hóa học là yếu tố quan trọng để dự đoán phản ứng hóa học.
Sản phẩm hữu ích: thể tích la gì lớp 5
Sản phẩm liên quan: hoa nhài ba lá
Sản phẩm hữu ích: năng lượng dao động điều hòa
Sản phẩm liên quan: cho rùa ăn bao nhiêu là đủ
Xem thêm: bài hát cỏ úa