Công thức Lewis của H2SO4
Chính Sách Vận Chuyển Và Đổi Trả Hàng
Miễn phí vận chuyển mọi đơn hàng từ 500K
- Phí ship mặc trong nước 50K
- Thời gian nhận hàng 2-3 ngày trong tuần
- Giao hàng hỏa tốc trong 24h
- Hoàn trả hàng trong 30 ngày nếu không hài lòng
Mô tả sản phẩm
Công thức Lewis của H2SO4 (axit sulfuric) thể hiện sự sắp xếp các electron hóa trị trong phân tử, giúp hiểu rõ liên kết giữa các nguyên tử. Để viết công thức Lewis của H2SO4, chúng ta cần xác định số electron hóa trị của mỗi nguyên tử. Lưu ý rằng lưu huỳnh (S) có khả năng mở rộng lớp vỏ hóa trị.
Các bước viết công thức Lewis của H2SO4
Bước 1: Tính tổng số electron hóa trị
Nguyên tử H có 1 electron hóa trị, O có 6 electron hóa trị và S có 6 electron hóa trị. Tổng số electron hóa trị trong H2SO4 là: (2 x 1) + (4 x 6) + 6 = 32 electron.
Bước 2: Xác định nguyên tử trung tâm
Lưu huỳnh (S) là nguyên tử trung tâm vì nó có độ âm điện thấp hơn oxi.
Bước 3: Vẽ khung cơ bản
Liên kết mỗi nguyên tử O với nguyên tử S bằng một liên kết đơn. Hai nguyên tử H liên kết với hai trong số các nguyên tử O.
Bước 4: Điền electron vào các nguyên tử ngoại vi
Điền các electron còn lại vào các nguyên tử O để mỗi nguyên tử O có 8 electron (ngoại trừ H chỉ cần 2 electron).
Bước 5: Kiểm tra số electron
Sau khi điền electron, ta thấy rằng lưu huỳnh chưa đạt octet (8 electron). Để hoàn thành octet cho lưu huỳnh, ta cần tạo liên kết đôi giữa lưu huỳnh và hai nguyên tử oxi.
Bước 6: Công thức Lewis hoàn chỉnh
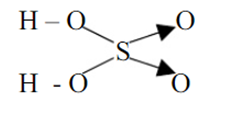
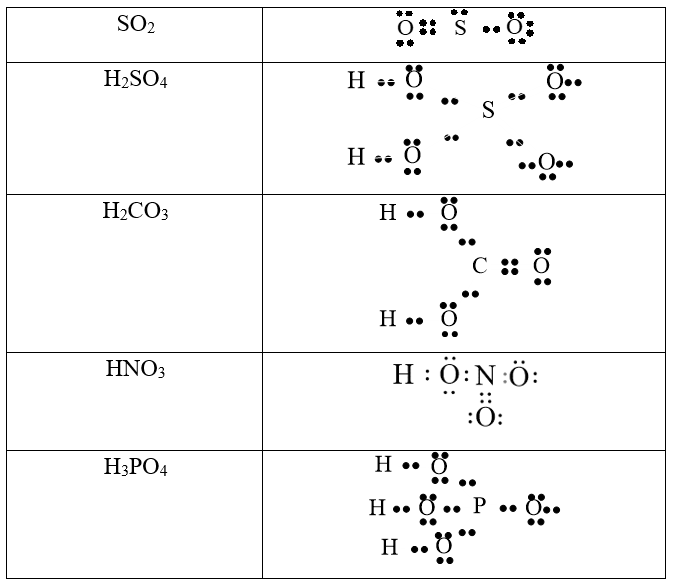
Công thức Lewis hoàn chỉnh của H2SO4 sẽ có hai liên kết đôi S=O và hai liên kết đơn S-O, với mỗi nguyên tử O liên kết đơn với S cũng liên kết với một nguyên tử H. Hai nguyên tử H chỉ có hai electron chia sẻ. Lưu huỳnh ở trung tâm có 12 electron xung quanh, do có khả năng mở rộng lớp vỏ điện tử.
Hình ảnh minh họa công thức Lewis của H2SO4 thường được tìm thấy trên các trang web hóa học hoặc sách giáo khoa. Việc vẽ công thức Lewis chính xác giúp hiểu rõ hơn về hình học phân tử và tính chất hóa học của H2SO4.
Sản phẩm hữu ích: bài thơ hay về mùa hè
Sản phẩm hữu ích: đại từ xưng hô tiếng anh
Xem thêm: bài học về ý chí nghị lực
Sản phẩm hữu ích: 1 hecta là bao nhiêu m2