Tốc độ phản ứng được xác định bởi độ biến thiên


Chính Sách Vận Chuyển Và Đổi Trả Hàng
Miễn phí vận chuyển mọi đơn hàng từ 500K
- Phí ship mặc trong nước 50K
- Thời gian nhận hàng 2-3 ngày trong tuần
- Giao hàng hỏa tốc trong 24h
- Hoàn trả hàng trong 30 ngày nếu không hài lòng
Mô tả sản phẩm
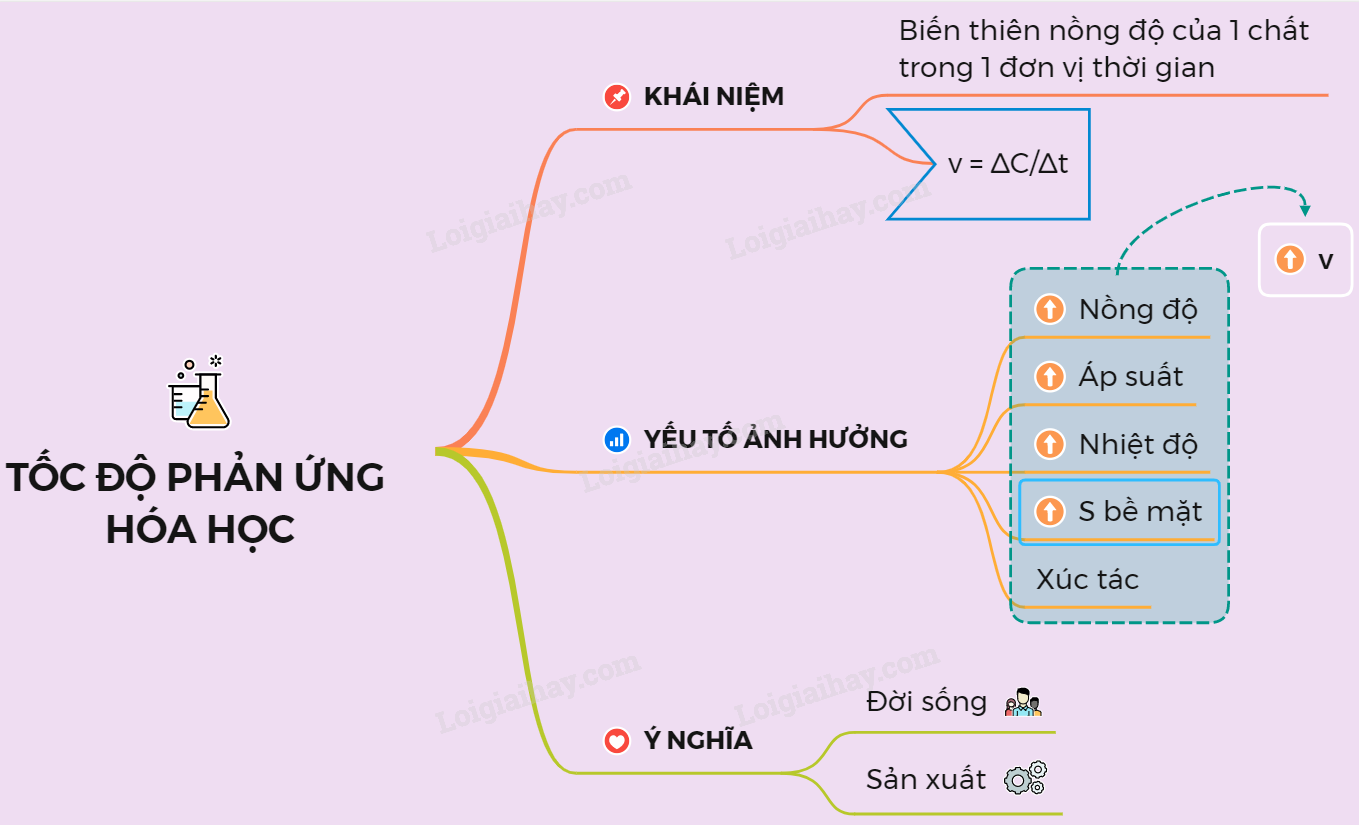
Tốc độ phản ứng được xác định bởi độ biến thiên của nồng độ chất phản ứng hoặc sản phẩm trong một đơn vị thời gian. Cụ thể, nó thể hiện sự thay đổi nhanh hay chậm của phản ứng hóa học.
Hiểu rõ về độ biến thiên trong tốc độ phản ứng
Độ biến thiên nồng độ
Độ biến thiên nồng độ là sự thay đổi nồng độ của chất phản ứng hoặc sản phẩm trong một khoảng thời gian nhất định. Đây là yếu tố chính được sử dụng để tính toán tốc độ phản ứng. Một sự giảm nồng độ chất phản ứng hoặc tăng nồng độ sản phẩm trong một khoảng thời gian ngắn cho thấy tốc độ phản ứng cao. Ngược lại, một sự thay đổi nhỏ trong cùng khoảng thời gian cho thấy tốc độ phản ứng thấp. Ví dụ, nếu nồng độ của một chất phản ứng giảm đi 0.1M trong 1 giây, tốc độ phản ứng sẽ là 0.1 M/s.
Độ biến thiên thời gian
Độ biến thiên thời gian là khoảng thời gian mà ta quan sát sự thay đổi nồng độ. Việc chọn khoảng thời gian thích hợp rất quan trọng để có kết quả chính xác. Khoảng thời gian quá ngắn có thể dẫn đến sai số do đo lường, trong khi khoảng thời gian quá dài có thể không phản ánh chính xác tốc độ phản ứng trong suốt quá trình.
Các yếu tố ảnh hưởng đến độ biến thiên và tốc độ phản ứng
Nồng độ chất phản ứng
Nồng độ chất phản ứng càng cao, tốc độ phản ứng càng nhanh. Điều này là do số lượng các phân tử chất phản ứng va chạm với nhau trong một đơn vị thời gian tăng lên, dẫn đến tăng xác suất xảy ra phản ứng.
Nhiệt độ
Nhiệt độ cao làm tăng năng lượng động của các phân tử, dẫn đến tăng số lượng va chạm hiệu quả và do đó tăng tốc độ phản ứng. Mỗi phản ứng thường có một năng lượng hoạt hóa, và nhiệt độ cao giúp các phân tử vượt qua được rào cản năng lượng này dễ dàng hơn.
Chất xúc tác
Chất xúc tác làm tăng tốc độ phản ứng bằng cách cung cấp một con đường phản ứng có năng lượng hoạt hóa thấp hơn. Chất xúc tác không bị tiêu hao trong quá trình phản ứng.
Diện tích bề mặt
Đối với các phản ứng xảy ra ở bề mặt, diện tích bề mặt càng lớn thì tốc độ phản ứng càng nhanh vì số lượng các phân tử tiếp xúc với bề mặt tăng lên.
Xem thêm: hình tô màu hoa quả
Xem thêm: tô màu thức ăn
Xem thêm: đặt câu hỏi cho bộ phận in đậm lớp 2 - tuần 27
Sản phẩm hữu ích: một hình tam giác abc có cạnh đáy 3 5m