Tính chất hóa học của nước lớp 8

Chính Sách Vận Chuyển Và Đổi Trả Hàng
Miễn phí vận chuyển mọi đơn hàng từ 500K
- Phí ship mặc trong nước 50K
- Thời gian nhận hàng 2-3 ngày trong tuần
- Giao hàng hỏa tốc trong 24h
- Hoàn trả hàng trong 30 ngày nếu không hài lòng
Mô tả sản phẩm
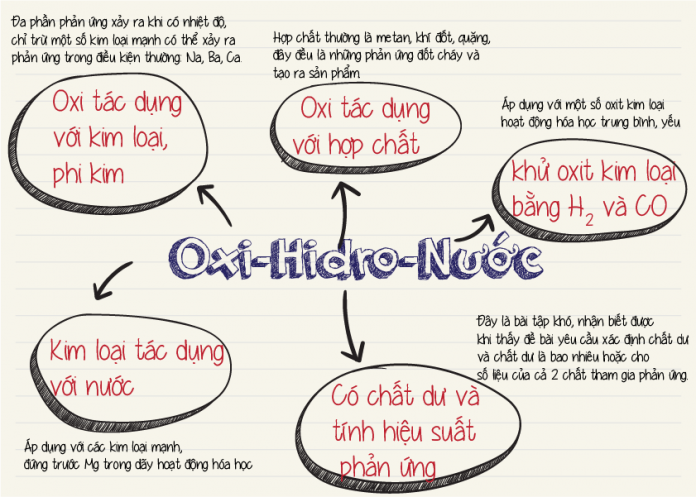
Nước (H₂O) không chỉ là dung môi phổ biến mà còn tham gia vào nhiều phản ứng hóa học quan trọng. Ở lớp 8, chúng ta tìm hiểu về một số tính chất hóa học cơ bản của nước.
Phản ứng của nước với kim loại
Tác dụng với kim loại hoạt động mạnh
Nước tác dụng với một số kim loại hoạt động mạnh như kali (K), natri (Na), canxi (Ca),… ở nhiệt độ thường tạo ra bazơ tương ứng và giải phóng khí hiđro. Ví dụ: 2Na + 2H₂O → 2NaOH + H₂↑ 2K + 2H₂O → 2KOH + H₂↑ Ca + 2H₂O → Ca(OH)₂ + H₂↑Tác dụng với kim loại hoạt động yếu hơn
Một số kim loại hoạt động yếu hơn như sắt (Fe), nhôm (Al),… chỉ phản ứng với nước ở nhiệt độ cao. Ví dụ: 3Fe + 4H₂O (t°) → Fe₃O₄ + 4H₂↑ 2Al + 3H₂O (t°) → Al₂O₃ + 3H₂↑Phản ứng của nước với oxit kim loại
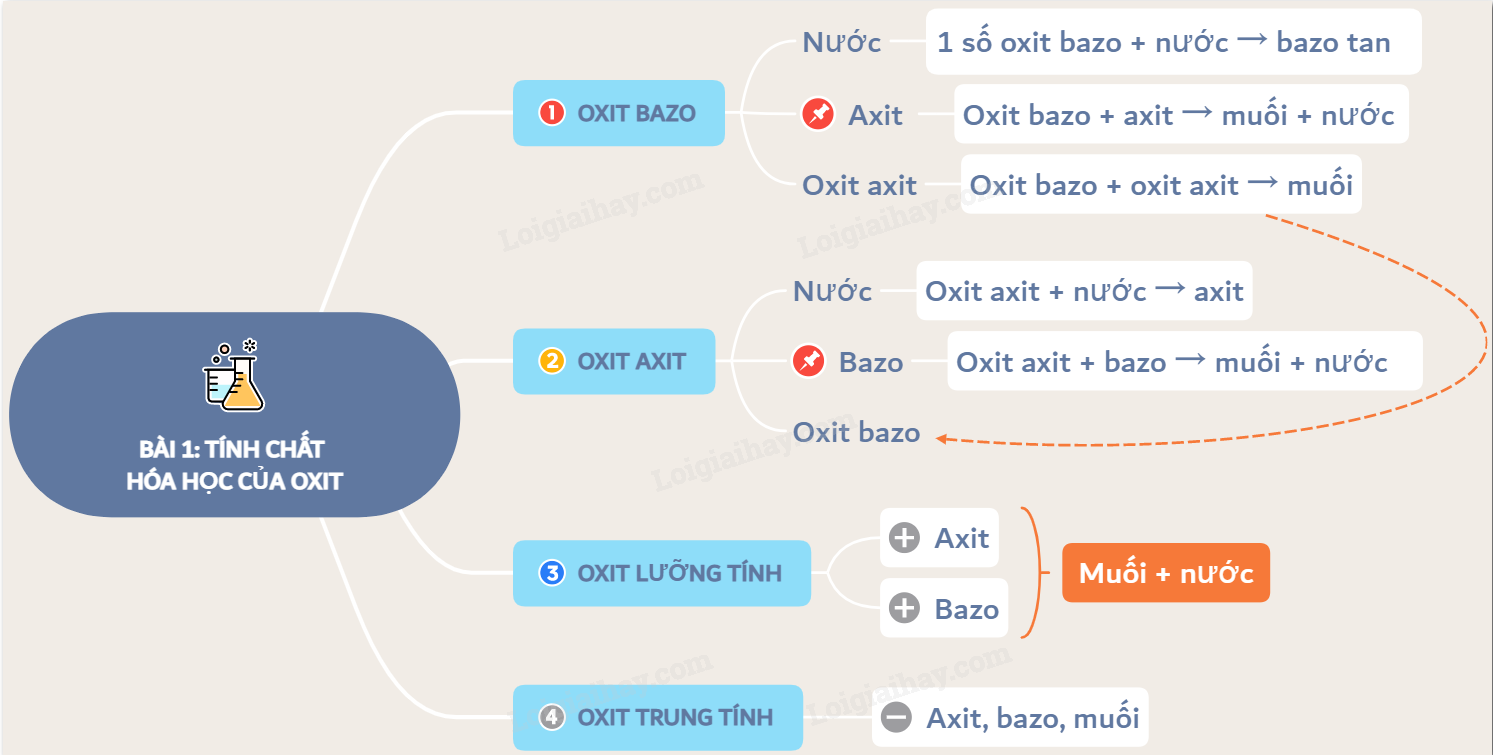
Nước tác dụng với một số oxit kim loại tạo ra bazơ tương ứng. Phản ứng này thường xảy ra với các oxit kim loại kiềm và kiềm thổ. Ví dụ: Na₂O + H₂O → 2NaOH CaO + H₂O → Ca(OH)₂ K₂O + H₂O → 2KOHPhản ứng của nước với oxit phi kim
Nước tác dụng với một số oxit phi kim tạo ra axit tương ứng. Ví dụ: SO₃ + H₂O → H₂SO₄ P₂O₅ + 3H₂O → 2H₃PO₄ CO₂ + H₂O ⇌ H₂CO₃ (phản ứng thuận nghịch) Tóm lại, nước thể hiện tính chất hóa học khá đa dạng, phản ứng với nhiều chất khác nhau tạo ra các sản phẩm khác nhau. Việc hiểu rõ các tính chất hóa học của nước là rất quan trọng trong việc giải thích nhiều hiện tượng tự nhiên và ứng dụng trong thực tiễn.Sản phẩm hữu ích: đề toán lớp 3 cánh diều
Sản phẩm liên quan: tại sao trạng thái đứng yên hay chuyển động của một vật có tính tương đối
Sản phẩm liên quan: quá trình oxi hóa là quá trình nào sau đây
Sản phẩm hữu ích: táo đỏ khô tiếng anh