SO2 + H2O + Br2: Phản ứng và Sản phẩm

Chính Sách Vận Chuyển Và Đổi Trả Hàng
Miễn phí vận chuyển mọi đơn hàng từ 500K
- Phí ship mặc trong nước 50K
- Thời gian nhận hàng 2-3 ngày trong tuần
- Giao hàng hỏa tốc trong 24h
- Hoàn trả hàng trong 30 ngày nếu không hài lòng
Mô tả sản phẩm
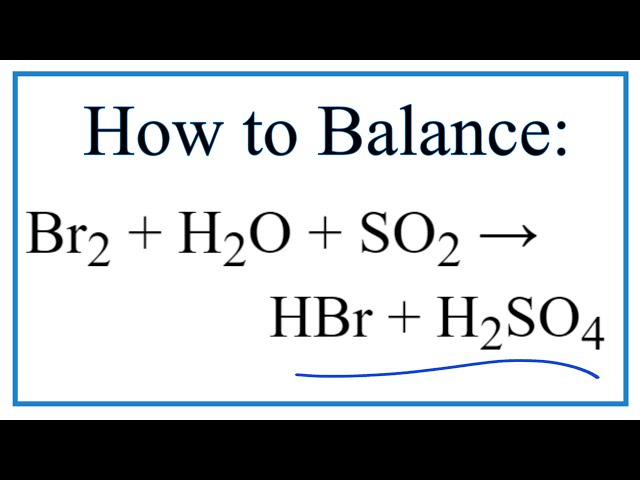
Phản ứng giữa SO2, H2O và Br2 tạo ra axit sunfuric (H2SO4) và axit bromhydric (HBr). SO2 đóng vai trò là chất khử, trong khi Br2 là chất oxi hóa. Nước đóng vai trò là môi trường phản ứng và tham gia vào quá trình tạo thành axit.
Cơ chế phản ứng SO2 + H2O + Br2
Sự oxi hóa SO2
Lưu huỳnh đioxit (SO2) là một chất khử, nó có xu hướng nhường electron. Trong phản ứng này, SO2 bị oxi hóa bởi brom (Br2) thành axit sunfuric (H2SO4).
Sự khử Br2
Brom (Br2) là chất oxi hóa, nó nhận electron từ SO2. Quá trình này dẫn đến sự hình thành axit bromhydric (HBr).
Phản ứng tổng thể
Phản ứng tổng thể có thể được viết như sau (cân bằng): SO2 + 2H2O + Br2 → H2SO4 + 2HBr. Tuy nhiên, phản ứng này thường diễn ra chậm và cần điều kiện xúc tác thích hợp để tăng tốc độ.
Ứng dụng và tầm quan trọng
Trong công nghiệp
Mặc dù phản ứng này không được sử dụng rộng rãi trong công nghiệp sản xuất H2SO4, hiểu biết về phản ứng này quan trọng trong việc kiểm soát và xử lý khí thải chứa SO2, giảm thiểu ô nhiễm môi trường.
Trong nghiên cứu
Phản ứng này có ý nghĩa trong nghiên cứu hóa học về phản ứng oxi hóa khử, đặc biệt là vai trò của SO2 như một chất khử và Br2 như một chất oxi hóa.
Các yếu tố ảnh hưởng đến phản ứng
Nồng độ chất phản ứng
Nồng độ của SO2, H2O và Br2 ảnh hưởng trực tiếp đến tốc độ phản ứng. Nồng độ cao hơn sẽ làm tăng tốc độ phản ứng.
Nhiệt độ
Nhiệt độ cũng là một yếu tố quan trọng. Tăng nhiệt độ thường làm tăng tốc độ phản ứng.
Chất xúc tác
Một số chất xúc tác có thể làm tăng tốc độ phản ứng này. Việc tìm kiếm và nghiên cứu chất xúc tác hiệu quả là một hướng nghiên cứu quan trọng.
Sản phẩm hữu ích: phân tử c 2 h 2 có chứa
Sản phẩm hữu ích: 283 bến vân đồn
Xem thêm: tchh của kim loại
Sản phẩm liên quan: bài hát kỷ niệm tuổi học trò