Phản ứng của kim loại S với H2SO4 loãng
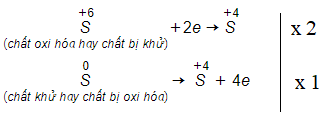
Chính Sách Vận Chuyển Và Đổi Trả Hàng
Miễn phí vận chuyển mọi đơn hàng từ 500K
- Phí ship mặc trong nước 50K
- Thời gian nhận hàng 2-3 ngày trong tuần
- Giao hàng hỏa tốc trong 24h
- Hoàn trả hàng trong 30 ngày nếu không hài lòng
Mô tả sản phẩm
Phản ứng của lưu huỳnh (S) với axit sunfuric loãng (H2SO4) không xảy ra. Lưu huỳnh là một phi kim, không phản ứng với axit loãng. Để phản ứng xảy ra, cần điều kiện khác khắc nghiệt hơn.
Điều kiện phản ứng của Lưu huỳnh với Axit
Lưu huỳnh không phản ứng với H2SO4 loãng
Lưu huỳnh là một phi kim có độ hoạt động hóa học tương đối thấp. Axit sunfuric loãng là một axit yếu, không đủ mạnh để oxi hóa lưu huỳnh. Do đó, phản ứng giữa lưu huỳnh và axit sunfuric loãng không xảy ra ở điều kiện thường.
Điều kiện cần thiết để lưu huỳnh phản ứng
Để lưu huỳnh có thể phản ứng, cần phải có các điều kiện mạnh hơn như:
- Axit sunfuric đặc, nóng: Trong điều kiện này, H2SO4 đặc đóng vai trò chất oxi hóa mạnh, oxi hóa lưu huỳnh thành lưu huỳnh đioxit (SO2) và tạo ra nước.
- Chất oxi hóa mạnh khác: Các chất oxi hóa mạnh khác như HNO3 đặc, nóng cũng có thể phản ứng với lưu huỳnh.
- Nhiệt độ cao: Nhiệt độ cao cung cấp năng lượng hoạt hóa cần thiết để phản ứng xảy ra.
Ví dụ về phản ứng của lưu huỳnh với các chất khác
Phản ứng với oxi
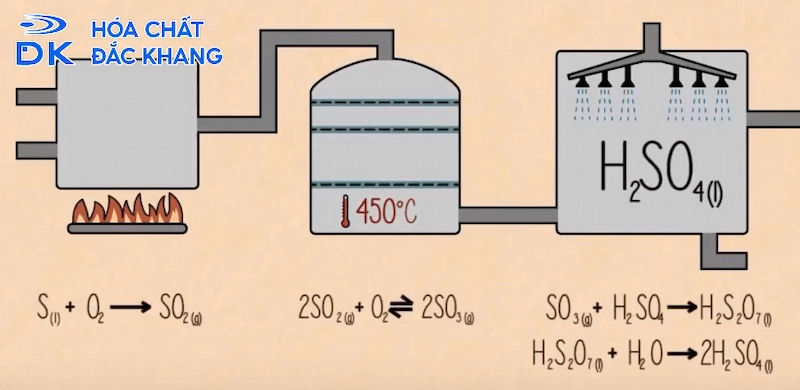
Lưu huỳnh cháy trong oxi tạo thành lưu huỳnh đioxit:
S + O2 → SO2
Phản ứng với kim loại
Lưu huỳnh phản ứng với nhiều kim loại tạo thành sunfua kim loại. Ví dụ:
Fe + S → FeS
Xem thêm: xoay ca là gì
Xem thêm: truyện ai đem ai là thật
Sản phẩm hữu ích: cách trồng cây ngải cứu
Sản phẩm liên quan: cờ tướng siêu khó
Sản phẩm liên quan: đường xá hay sá