Phản ứng oxi hóa khử là gì?
Chính Sách Vận Chuyển Và Đổi Trả Hàng
Miễn phí vận chuyển mọi đơn hàng từ 500K
- Phí ship mặc trong nước 50K
- Thời gian nhận hàng 2-3 ngày trong tuần
- Giao hàng hỏa tốc trong 24h
- Hoàn trả hàng trong 30 ngày nếu không hài lòng
Mô tả sản phẩm
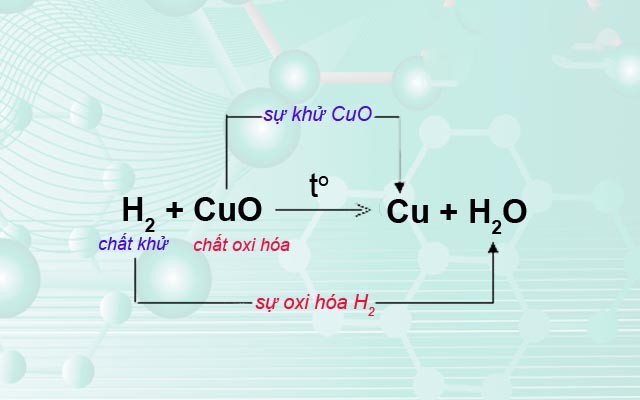
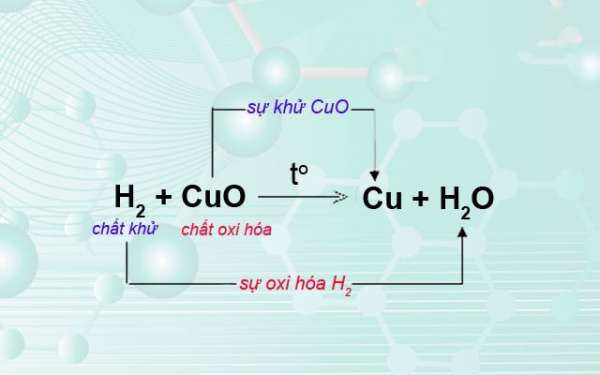
Phản ứng oxi hóa khử là phản ứng hóa học trong đó xảy ra sự chuyển electron giữa các chất tham gia phản ứng. Một chất nhường electron gọi là chất khử, đồng thời bị oxi hóa. Chất nhận electron gọi là chất oxi hóa, đồng thời bị khử.
Quá trình oxi hóa và khử
Oxi hóa
Oxi hóa là quá trình một chất mất electron. Trong quá trình này, số oxi hóa của nguyên tố tăng lên. Ví dụ, khi sắt (Fe) phản ứng với oxi (O2) tạo thành sắt oxit (Fe2O3), sắt bị oxi hóa vì nó mất electron.
Khử
Khử là quá trình một chất nhận electron. Trong quá trình này, số oxi hóa của nguyên tố giảm xuống. Ví dụ, trong phản ứng trên, oxi bị khử vì nó nhận electron từ sắt.
Đặc điểm của phản ứng oxi hóa khử
Các phản ứng oxi hóa khử luôn xảy ra đồng thời cả quá trình oxi hóa và quá trình khử. Số electron mà chất khử nhường phải bằng số electron mà chất oxi hóa nhận. Sự thay đổi số oxi hóa của các nguyên tố tham gia phản ứng là dấu hiệu nhận biết phản ứng oxi hóa khử.
Ví dụ về phản ứng oxi hóa khử
Phản ứng giữa kim loại với phi kim là một ví dụ điển hình cho phản ứng oxi hóa khử. Ví dụ: 2Na + Cl2 → 2NaCl. Trong phản ứng này, Na là chất khử (bị oxi hóa) và Cl2 là chất oxi hóa (bị khử).
Ứng dụng của phản ứng oxi hóa khử
Phản ứng oxi hóa khử có ứng dụng rất rộng rãi trong nhiều lĩnh vực, bao gồm: pin điện hóa, công nghiệp luyện kim, sản xuất phân bón, xử lý nước thải, …
Xem thêm: quãng đường vận tốc thời gian
Xem thêm: ôn tập toán lớp 4 học kì 1
Xem thêm: luyện gõ bàn phím trên điện thoại
Sản phẩm liên quan: alu ngoài trời và alu trong nhà
Sản phẩm hữu ích: mô hình mút xốp