Oxit Bazơ Gồm Những Chất Nào?

Chính Sách Vận Chuyển Và Đổi Trả Hàng
Miễn phí vận chuyển mọi đơn hàng từ 500K
- Phí ship mặc trong nước 50K
- Thời gian nhận hàng 2-3 ngày trong tuần
- Giao hàng hỏa tốc trong 24h
- Hoàn trả hàng trong 30 ngày nếu không hài lòng
Mô tả sản phẩm
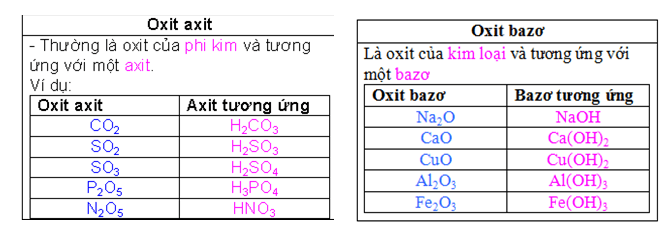
Oxit bazơ là những hợp chất gồm hai nguyên tố, trong đó có một nguyên tố là oxi và nguyên tố còn lại là một kim loại.
Phân loại Oxit Bazơ
Oxit bazơ tan trong nước:
Oxit bazơ tan trong nước tạo thành dung dịch bazơ (kiềm). Ví dụ điển hình là các oxit của kim loại kiềm (nhóm IA) như Na2O (natri oxit), K2O (kali oxit), Li2O (liti oxit),... và một số oxit của kim loại kiềm thổ (nhóm IIA) như CaO (canxi oxit), BaO (bari oxit),... Những oxit này phản ứng với nước tạo ra các bazơ tương ứng, ví dụ: Na2O + H2O → 2NaOH.Oxit bazơ không tan trong nước:
Phần lớn các oxit bazơ không tan trong nước. Ví dụ như CuO (đồng(II) oxit), Fe2O3 (sắt(III) oxit), MgO (magie oxit), Al2O3 (nhôm oxit), ZnO (kẽm oxit),... Chúng thường phản ứng với axit tạo thành muối và nước.Ví dụ về một số Oxit Bazơ thường gặp
Dưới đây là một số ví dụ về oxit bazơ thường gặp trong chương trình hóa học phổ thông:
- Na2O: Natri oxit
- K2O: Kali oxit
- CaO: Canxi oxit (vôi sống)
- MgO: Magie oxit
- FeO: Sắt(II) oxit
- Fe2O3: Sắt(III) oxit
- CuO: Đồng(II) oxit
- ZnO: Kẽm oxit
- Al2O3: Nhôm oxit
Lưu ý: Danh sách trên không đầy đủ, còn rất nhiều oxit bazơ khác nữa. Tùy thuộc vào mức độ học tập mà bạn sẽ tiếp xúc với nhiều oxit bazơ hơn.
Sản phẩm liên quan: ánh sáng đỏ có tác dụng gì
Sản phẩm hữu ích: áp suất không khí là gì
Sản phẩm hữu ích: tính chất của oxit axit
Sản phẩm hữu ích: cách trị rệp trắng trên cây
Xem thêm: oxit nào sau đây là oxit trung tính