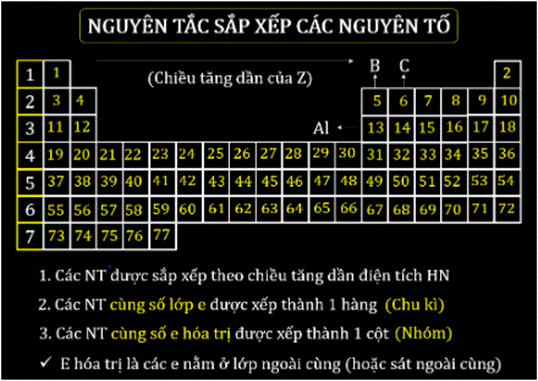
Nguyên tắc sắp xếp các nguyên tố hóa học trong bảng tuần hoàn
Chính Sách Vận Chuyển Và Đổi Trả Hàng
Miễn phí vận chuyển mọi đơn hàng từ 500K
- Phí ship mặc trong nước 50K
- Thời gian nhận hàng 2-3 ngày trong tuần
- Giao hàng hỏa tốc trong 24h
- Hoàn trả hàng trong 30 ngày nếu không hài lòng
Mô tả sản phẩm
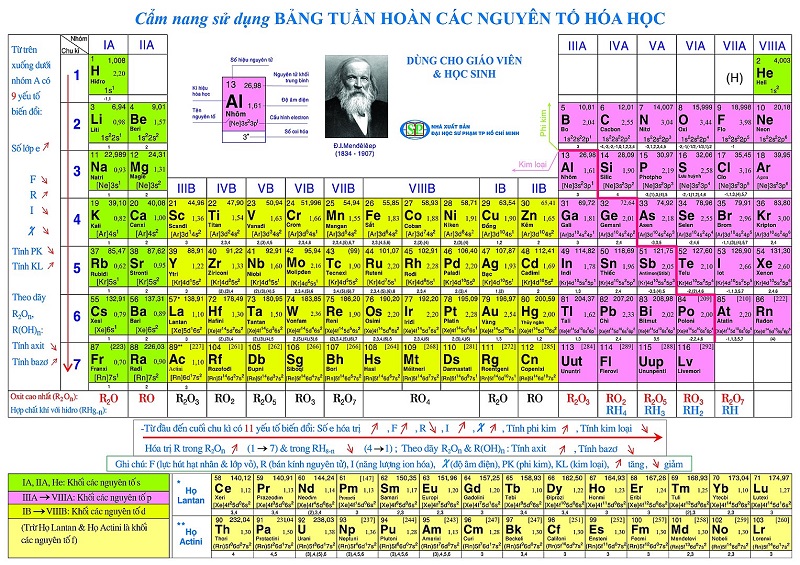
Bảng tuần hoàn các nguyên tố hóa học được sắp xếp dựa trên số nguyên tử và cấu hình electron của các nguyên tố. Nói một cách đơn giản, các nguyên tố được sắp xếp theo chiều tăng dần của số nguyên tử, đồng thời nhóm các nguyên tố có tính chất hóa học tương tự nhau vào cùng một cột (nhóm).
Số nguyên tử và cấu hình electron
Số nguyên tử:
Nguyên tắc cơ bản nhất là sắp xếp các nguyên tố theo thứ tự tăng dần của số nguyên tử (Z), đại diện cho số proton trong hạt nhân nguyên tử. Số proton quyết định bản chất hóa học của nguyên tố.Cấu hình electron:
Cấu hình electron của nguyên tố xác định vị trí của nó trong bảng tuần hoàn. Các nguyên tố cùng nhóm có cấu hình electron lớp ngoài cùng tương tự nhau, dẫn đến tính chất hóa học tương đồng. Ví dụ, các nguyên tố nhóm IA (kim loại kiềm) đều có cấu hình electron lớp ngoài cùng là ns1, cho nên chúng đều có tính khử mạnh.Chu kỳ và nhóm
Chu kỳ:
Các nguyên tố được sắp xếp thành hàng ngang gọi là chu kỳ. Số chu kỳ tương ứng với số lớp electron trong nguyên tử. Các nguyên tố trong cùng một chu kỳ có số lớp electron bằng nhau nhưng số electron lớp ngoài cùng khác nhau.Nhóm:
Các nguyên tố được sắp xếp thành cột dọc gọi là nhóm. Các nguyên tố cùng nhóm có cấu hình electron lớp ngoài cùng tương tự nhau, dẫn đến tính chất hóa học tương tự. Ví dụ, các nguyên tố nhóm VIIIA (khí hiếm) có cấu hình electron lớp ngoài cùng là ns2np6 (trừ He), do đó chúng rất trơ về mặt hóa học.Sự lặp lại tính chất
Sự sắp xếp này làm nổi bật sự tuần hoàn của tính chất hóa học của các nguyên tố. Khi di chuyển qua các chu kỳ và nhóm, tính chất hóa học như độ âm điện, tính kim loại/phi kim, bán kính nguyên tử… sẽ thay đổi theo chu kỳ. Sự tuần hoàn này là cơ sở cho việc dự đoán và giải thích tính chất của các nguyên tố chưa được biết đến.Sản phẩm liên quan: phim việt nam cần một bờ vai tập cuối
Xem thêm: vẽ cáo chín đuôi
Sản phẩm hữu ích: cảm ơn em đã sưởi ấm anh
Sản phẩm liên quan: tác dụng cây húng chanh
Sản phẩm hữu ích: đề ôn thi lớp 3