Lý thuyết Sắt và Hợp chất của Sắt

Chính Sách Vận Chuyển Và Đổi Trả Hàng
Miễn phí vận chuyển mọi đơn hàng từ 500K
- Phí ship mặc trong nước 50K
- Thời gian nhận hàng 2-3 ngày trong tuần
- Giao hàng hỏa tốc trong 24h
- Hoàn trả hàng trong 30 ngày nếu không hài lòng
Mô tả sản phẩm
Bạn đang tìm hiểu về lý thuyết sắt và hợp chất của sắt? Bài viết này sẽ cung cấp cho bạn kiến thức toàn diện về nguyên tố sắt, từ tính chất vật lý, hóa học đến các hợp chất quan trọng và ứng dụng của chúng trong đời sống. Chúng ta sẽ cùng tìm hiểu về sắt và các hợp chất phổ biến của nó một cách chi tiết và dễ hiểu.
Tính chất của Sắt
Tính chất vật lý:
Sắt là kim loại màu trắng xám, có ánh kim, khá cứng, dẻo, dễ rèn, dễ dát mỏng và kéo thành sợi. Sắt có khối lượng riêng 7,87 g/cm³, nhiệt độ nóng chảy 1539°C và nhiệt độ sôi 2862°C. Sắt dẫn điện và dẫn nhiệt tốt.Tính chất hóa học:
Sắt là kim loại hoạt động hoá học khá mạnh. Trong các phản ứng hóa học, sắt có thể thể hiện số oxi hoá +2 hoặc +3. Sắt tác dụng với phi kim (oxi, clo, lưu huỳnh…), tác dụng với dung dịch axit (HCl, H2SO4 loãng…), tác dụng với muối của kim loại kém hoạt động hơn. Hiện tượng thụ động hóa của sắt cũng cần được lưu ý.Hợp chất quan trọng của Sắt
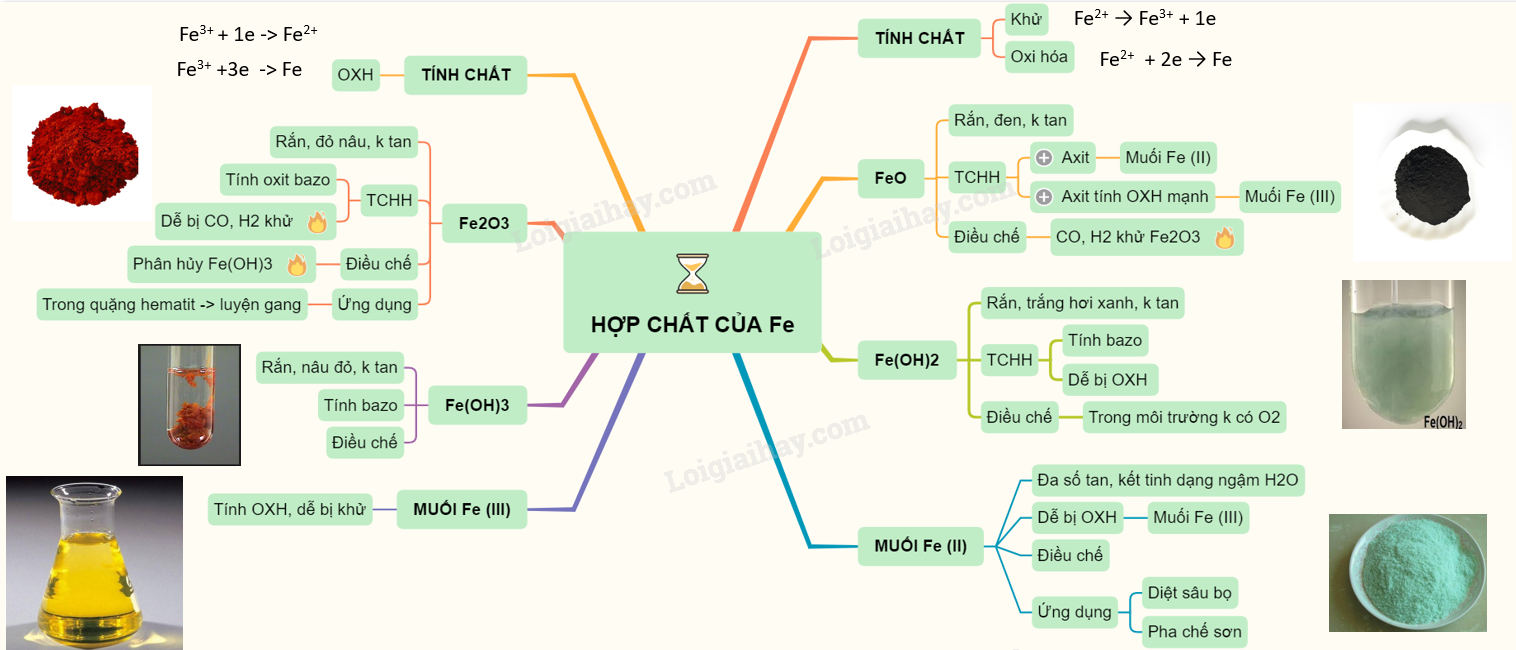
Oxit sắt:
Sắt tạo ra nhiều oxit khác nhau, trong đó FeO (sắt(II) oxit), Fe2O3 (sắt(III) oxit) và Fe3O4 (oxit sắt từ) là phổ biến nhất. Mỗi oxit có những tính chất hóa học và ứng dụng riêng biệt. Ví dụ, Fe2O3 được sử dụng rộng rãi làm chất tạo màu trong công nghiệp sơn.Muối sắt:
Sắt tạo ra nhiều loại muối khác nhau, ví dụ như sắt(II) sunfat (FeSO4), sắt(III) clorua (FeCl3),… Những muối này có nhiều ứng dụng khác nhau trong công nghiệp và y tế.Sunfua sắt:
Sắt tạo ra các sunfua như FeS (sắt(II) sunfua) và FeS2 (pirit sắt). FeS2 là nguyên liệu quan trọng để sản xuất axit sunfuric.Ứng dụng của Sắt và Hợp chất của Sắt
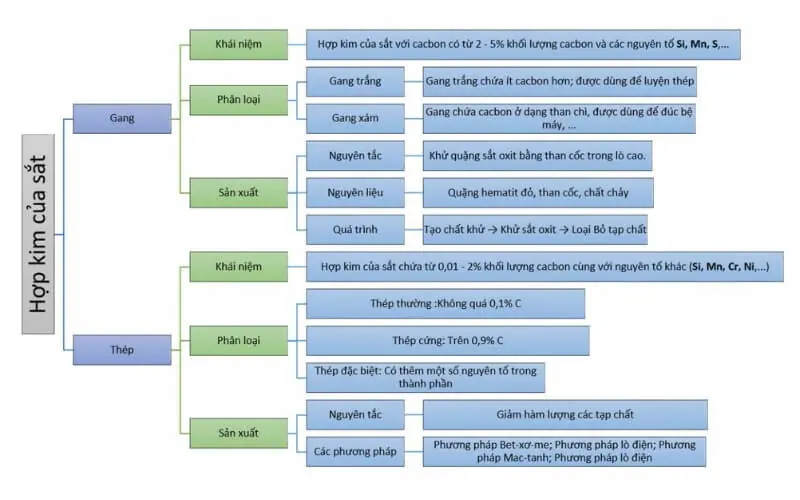
Sắt và hợp chất của sắt có ứng dụng vô cùng rộng rãi trong nhiều lĩnh vực, từ xây dựng, chế tạo máy móc, sản xuất ô tô, đến y tế và công nghiệp hóa chất.Phương pháp điều chế Sắt
Sắt được điều chế chủ yếu bằng phương pháp luyện kim, thông qua quá trình khử quặng sắt oxit bằng cacbon trong lò cao.Xem thêm: wound up là gì
Sản phẩm liên quan: down round là gì
Sản phẩm liên quan: 94 và 97 có hợp không