Liên kết cộng hóa trị và liên kết ion
Chính Sách Vận Chuyển Và Đổi Trả Hàng
Miễn phí vận chuyển mọi đơn hàng từ 500K
- Phí ship mặc trong nước 50K
- Thời gian nhận hàng 2-3 ngày trong tuần
- Giao hàng hỏa tốc trong 24h
- Hoàn trả hàng trong 30 ngày nếu không hài lòng
Mô tả sản phẩm
Liên kết cộng hóa trị và liên kết ion là hai loại liên kết hóa học chính giữ các nguyên tử lại với nhau tạo thành phân tử và hợp chất. Sự khác biệt chính giữa chúng nằm ở cách các nguyên tử chia sẻ hoặc chuyển giao electron. Liên kết cộng hóa trị hình thành khi các nguyên tử chia sẻ electron, trong khi liên kết ion hình thành khi một nguyên tử chuyển giao electron cho nguyên tử khác.
Sự khác biệt giữa liên kết cộng hóa trị và liên kết ion
Bản chất của liên kết
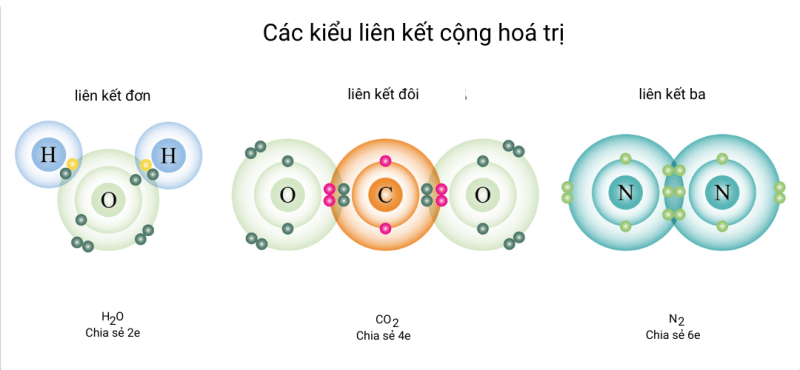
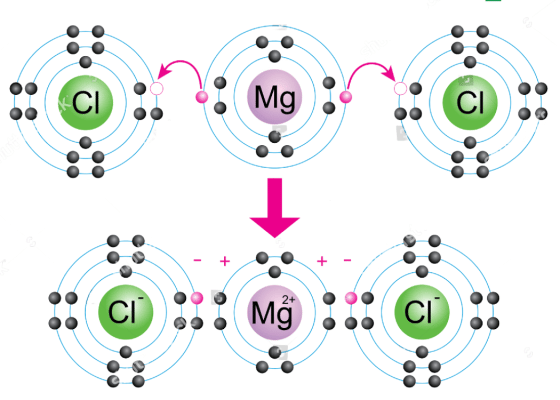
Liên kết cộng hóa trị là sự chia sẻ một hoặc nhiều cặp electron giữa hai nguyên tử phi kim. Các nguyên tử liên kết với nhau bằng cách tạo ra các cặp electron chung, thu được cấu hình electron bền vững giống như khí hiếm. Ví dụ điển hình là phân tử nước (H₂O), mỗi nguyên tử hydro chia sẻ một cặp electron với nguyên tử oxy. Ngược lại, liên kết ion là sự chuyển giao electron từ một nguyên tử kim loại cho một nguyên tử phi kim. Nguyên tử kim loại mất electron để tạo thành ion dương (cation), trong khi nguyên tử phi kim nhận electron để tạo thành ion âm (anion). Sự hút tĩnh điện giữa các ion trái dấu này tạo nên liên kết ion. Ví dụ: Natri clorua (NaCl), natri (kim loại) cho một electron cho clo (phi kim) tạo ra Na+ và Cl-.
Tính chất của hợp chất
Hợp chất cộng hóa trị thường tồn tại ở dạng phân tử rời rạc, có nhiệt độ nóng chảy và sôi thấp, thường không dẫn điện khi ở trạng thái rắn hoặc lỏng. Hợp chất ion thường tồn tại ở dạng tinh thể ion, có nhiệt độ nóng chảy và sôi cao, và dẫn điện khi nóng chảy hoặc hòa tan trong nước.
Độ âm điện
Độ chênh lệch độ âm điện giữa các nguyên tử tham gia liên kết là một yếu tố quan trọng để xác định loại liên kết. Liên kết cộng hóa trị thường xảy ra giữa các nguyên tử có độ âm điện gần bằng nhau, trong khi liên kết ion xảy ra giữa các nguyên tử có độ âm điện chênh lệch lớn. Tuy nhiên, cũng có những trường hợp liên kết cộng hóa trị phân cực, trong đó độ âm điện của các nguyên tử không hoàn toàn bằng nhau, dẫn đến sự phân bố electron không đồng đều trong phân tử.
Ví dụ
Liên kết cộng hóa trị: H₂, O₂, N₂, CH₄, CO₂, HCl.
Liên kết ion: NaCl, KCl, MgO, CaCl₂, Al₂O₃.
Sản phẩm liên quan: hậu quả của suy giảm tầng ozon
Sản phẩm liên quan: vẽ tranh về bác hồ
Sản phẩm hữu ích: nguyên nhân đồng bị oxi hóa
Sản phẩm hữu ích: nguyên liệu làm xi măng