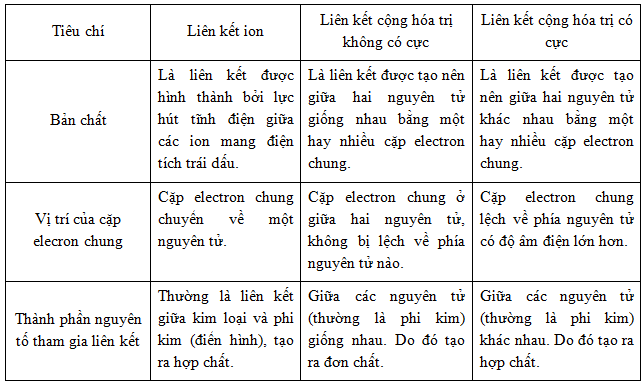
Liên kết cộng hóa trị khác với liên kết ion như thế nào?
Chính Sách Vận Chuyển Và Đổi Trả Hàng
Miễn phí vận chuyển mọi đơn hàng từ 500K
- Phí ship mặc trong nước 50K
- Thời gian nhận hàng 2-3 ngày trong tuần
- Giao hàng hỏa tốc trong 24h
- Hoàn trả hàng trong 30 ngày nếu không hài lòng
Mô tả sản phẩm
Liên kết cộng hóa trị và liên kết ion là hai loại liên kết hóa học chính, nhưng chúng khác nhau đáng kể về cách thức hình thành và đặc tính của các hợp chất tạo ra. Sự khác biệt chính nằm ở việc các nguyên tử chia sẻ hay chuyển electron.
Sự khác biệt cơ bản giữa liên kết cộng hóa trị và liên kết ion
Cơ chế hình thành liên kết:
Sự hình thành liên kết ion xảy ra khi một nguyên tử kim loại (có xu hướng mất electron) chuyển electron(s) sang một nguyên tử phi kim (có xu hướng nhận electron). Điều này tạo ra các ion mang điện tích trái dấu (cation dương và anion âm) hút nhau bằng lực tĩnh điện, tạo nên liên kết ion. Ngược lại, liên kết cộng hóa trị hình thành khi hai nguyên tử phi kim chia sẻ các electron hóa trị với nhau để đạt được cấu hình electron bền vững của khí hiếm.Tính chất của hợp chất:
Hợp chất ion thường là chất rắn ở nhiệt độ phòng, có nhiệt độ nóng chảy và sôi cao, giòn và dễ tan trong nước. Chúng dẫn điện khi nóng chảy hoặc hòa tan trong dung dịch. Hợp chất cộng hóa trị thường tồn tại ở các trạng thái vật chất khác nhau (rắn, lỏng, khí) tùy thuộc vào khối lượng phân tử và lực tương tác liên phân tử. Chúng thường có nhiệt độ nóng chảy và sôi thấp hơn hợp chất ion và không dẫn điện khi ở dạng tinh khiết.Ví dụ:
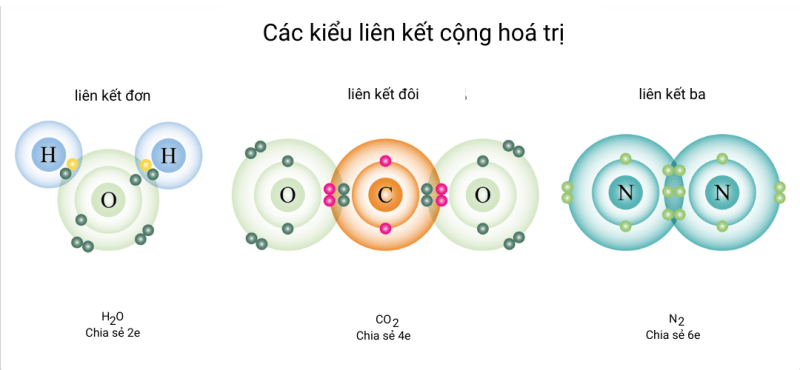
NaCl (natri clorua) là một ví dụ điển hình về hợp chất ion, trong đó natri (Na) mất một electron để tạo thành ion Na+ và clo (Cl) nhận electron đó để tạo thành ion Cl-. Trong khi đó, nước (H₂O) là một ví dụ về hợp chất cộng hóa trị, trong đó mỗi nguyên tử hydro chia sẻ một cặp electron với nguyên tử oxy.Sự khác biệt về độ phân cực:
Liên kết ion thường có độ phân cực rất cao do sự chênh lệch độ âm điện lớn giữa kim loại và phi kim. Liên kết cộng hóa trị có thể không phân cực (khi hai nguyên tử giống nhau chia sẻ electron) hoặc phân cực (khi hai nguyên tử khác nhau chia sẻ electron, nguyên tử có độ âm điện lớn hơn sẽ hút cặp electron mạnh hơn). Tóm lại, sự khác biệt chính giữa liên kết cộng hóa trị và liên kết ion nằm ở cách thức các nguyên tử liên kết với nhau: chuyển electron (ion) hay chia sẻ electron (cộng hóa trị). Hiểu được sự khác biệt này rất quan trọng để dự đoán tính chất và đặc điểm của các hợp chất hóa học.Sản phẩm hữu ích: al + koh dư
Xem thêm: trình bày tính chất
Sản phẩm hữu ích: quy tắc nhân chia cộng trừ
Xem thêm: áp suất khí quyển là gì
Sản phẩm liên quan: tranh truyện thỏ con không vâng lời