Điều Kiện Phản Ứng Là Gì?
Chính Sách Vận Chuyển Và Đổi Trả Hàng
Miễn phí vận chuyển mọi đơn hàng từ 500K
- Phí ship mặc trong nước 50K
- Thời gian nhận hàng 2-3 ngày trong tuần
- Giao hàng hỏa tốc trong 24h
- Hoàn trả hàng trong 30 ngày nếu không hài lòng
Mô tả sản phẩm
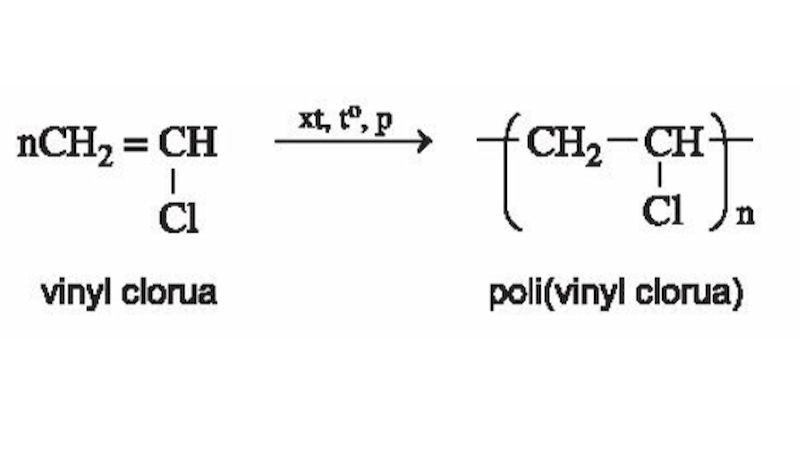
Điều kiện phản ứng là những yếu tố ảnh hưởng đến tốc độ và khả năng xảy ra của một phản ứng hóa học. Chúng bao gồm nhiệt độ, áp suất, nồng độ chất phản ứng, chất xúc tác và diện tích tiếp xúc. Hiểu rõ các điều kiện phản ứng giúp chúng ta kiểm soát và tối ưu hóa quá trình phản ứng.
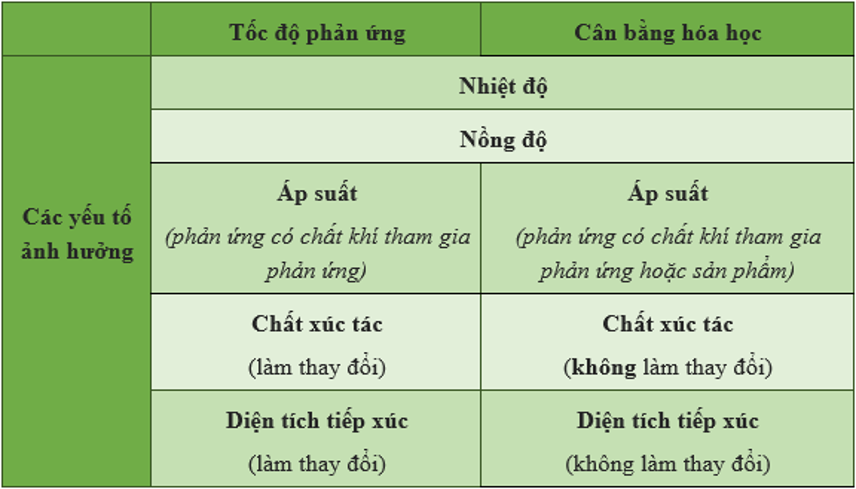
Các Yếu Tố Ảnh Hưởng Đến Điều Kiện Phản Ứng
Nhiệt độ:
Nhiệt độ cao thường làm tăng tốc độ phản ứng vì cung cấp năng lượng hoạt hóa cần thiết cho phản ứng xảy ra. Tuy nhiên, với một số phản ứng, nhiệt độ quá cao có thể gây ra phản ứng phụ không mong muốn.Áp suất:
Áp suất ảnh hưởng đáng kể đến các phản ứng khí. Tăng áp suất làm tăng nồng độ các chất khí, dẫn đến tăng tốc độ phản ứng. Đối với phản ứng chất rắn hoặc lỏng, áp suất thường ít ảnh hưởng hơn.Nồng độ chất phản ứng:
Nồng độ chất phản ứng càng cao, tốc độ phản ứng càng nhanh. Điều này là vì số lượng va chạm giữa các phân tử chất phản ứng tăng lên, làm tăng xác suất xảy ra phản ứng.Chất xúc tác:
Chất xúc tác là chất làm tăng tốc độ phản ứng mà không bị tiêu hao trong quá trình phản ứng. Chúng hoạt động bằng cách cung cấp một con đường phản ứng có năng lượng hoạt hóa thấp hơn.Diện tích tiếp xúc:
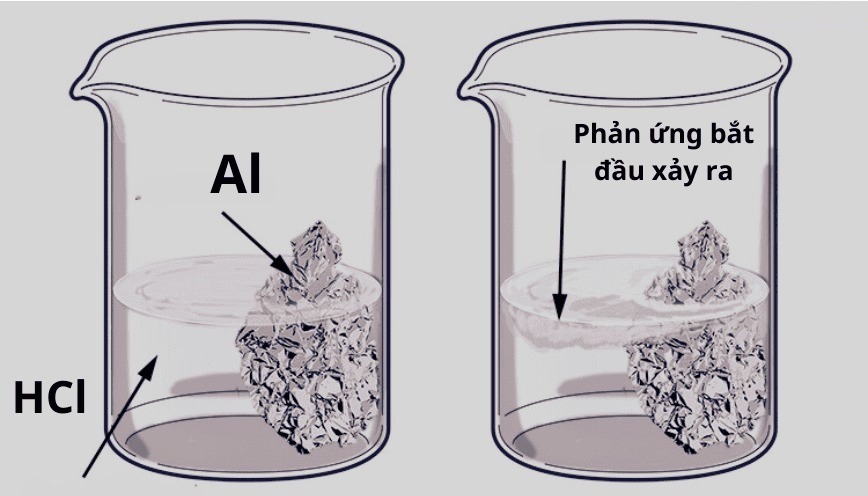
Diện tích tiếp xúc giữa các chất phản ứng càng lớn, tốc độ phản ứng càng nhanh. Ví dụ, bột Mg phản ứng với acid nhanh hơn so với một thanh Mg nguyên khối cùng khối lượng.Sản phẩm liên quan: bài tập lớp 3 tiếng anh
Sản phẩm hữu ích: mol là lượng chất chứa
Sản phẩm hữu ích: bìa nhựa đựng hồ sơ
Sản phẩm liên quan: nguyệt thực xảy ra khi nào ở việt nam