Dẫn Cl2 vào 200g dung dịch KBr
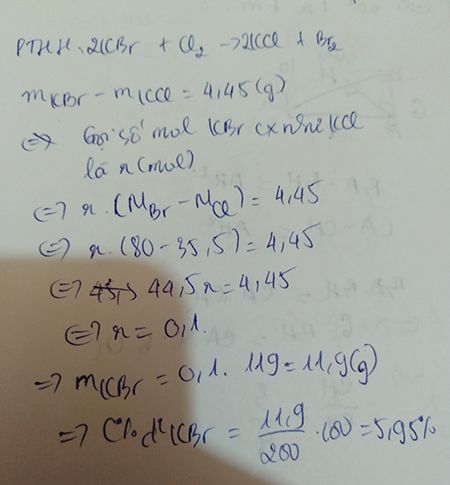

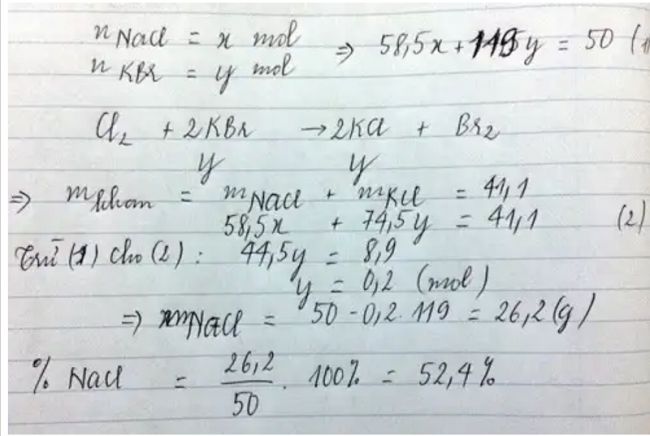
Chính Sách Vận Chuyển Và Đổi Trả Hàng
Miễn phí vận chuyển mọi đơn hàng từ 500K
- Phí ship mặc trong nước 50K
- Thời gian nhận hàng 2-3 ngày trong tuần
- Giao hàng hỏa tốc trong 24h
- Hoàn trả hàng trong 30 ngày nếu không hài lòng
Mô tả sản phẩm
Khi dẫn khí clo (Cl2) vào dung dịch kali bromua (KBr), sẽ xảy ra phản ứng oxi hóa khử. Clo (Cl2) có tính oxi hóa mạnh hơn brom (Br2), do đó nó sẽ oxi hóa ion bromua (Br-) thành brom (Br2) và tạo thành ion clorua (Cl-). Phản ứng được biểu diễn bằng phương trình hóa học sau:
Phản ứng hóa học
Phương trình ion
Cl2 + 2Br- → 2Cl- + Br2
Phương trình phân tử
Cl2 + 2KBr → 2KCl + Br2
Kết quả là dung dịch ban đầu không màu sẽ chuyển sang màu nâu đỏ đặc trưng của brom. Khối lượng dung dịch sau phản ứng sẽ phụ thuộc vào lượng Cl2 dẫn vào và lượng KBr ban đầu. Nếu Cl2 dư, phản ứng sẽ xảy ra hoàn toàn và tất cả ion Br- sẽ bị oxi hóa. Nếu Cl2 không dư, phản ứng sẽ không xảy ra hoàn toàn và một phần ion Br- sẽ còn lại. Để tính toán chính xác khối lượng dung dịch sau phản ứng, cần biết nồng độ của dung dịch KBr ban đầu và lượng Cl2 đã được dẫn vào. Bạn cần cung cấp thêm thông tin để tính toán cụ thể. Ví dụ, bạn cần biết nồng độ % của dung dịch KBr 200g hoặc số mol KBr trong 200g dung dịch.Ứng dụng
Phản ứng này được ứng dụng trong nhiều lĩnh vực, ví dụ như trong việc điều chế brom trong phòng thí nghiệm hoặc công nghiệp. Hiểu rõ phản ứng này giúp chúng ta hiểu về tính chất hóa học của halogen và ứng dụng của chúng.
Sản phẩm liên quan: c2h5oh + cuo đun nóng
Xem thêm: bài thơ cô dạy con
Xem thêm: bai tho meo di cau ca