Cấu tạo nguyên tử lớp 7
Chính Sách Vận Chuyển Và Đổi Trả Hàng
Miễn phí vận chuyển mọi đơn hàng từ 500K
- Phí ship mặc trong nước 50K
- Thời gian nhận hàng 2-3 ngày trong tuần
- Giao hàng hỏa tốc trong 24h
- Hoàn trả hàng trong 30 ngày nếu không hài lòng
Mô tả sản phẩm
Cấu tạo nguyên tử lớp 7 được mô tả đơn giản như sau: Nguyên tử gồm hạt nhân mang điện tích dương và các electron mang điện tích âm chuyển động xung quanh hạt nhân. Hạt nhân lại gồm proton mang điện tích dương và neutron không mang điện.
Mô hình hành tinh nguyên tử
Hạt nhân và electron
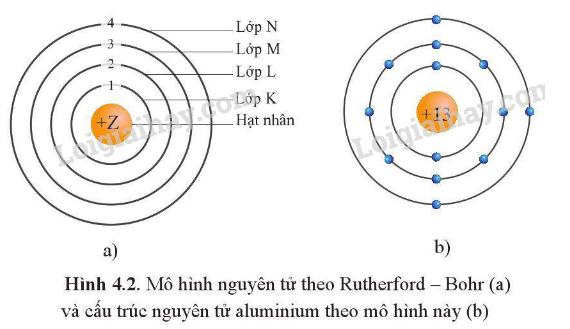
Mô hình nguyên tử đơn giản nhất mà các em học ở lớp 7 là mô hình hành tinh. Theo mô hình này, nguyên tử giống như hệ mặt trời thu nhỏ, với hạt nhân ở giữa đóng vai trò như mặt trời, mang điện tích dương do các proton cấu tạo nên. Xung quanh hạt nhân là các electron mang điện tích âm chuyển động trên các quỹ đạo giống như các hành tinh quay quanh mặt trời. Số lượng proton trong hạt nhân quyết định số hiệu nguyên tử và loại nguyên tố. Neutron, cũng nằm trong hạt nhân, không mang điện và giúp ổn định hạt nhân.
Sự khác biệt giữa proton, neutron và electron
Proton và neutron có khối lượng gần bằng nhau và lớn hơn rất nhiều so với electron. Electron có khối lượng rất nhỏ, gần như không đáng kể so với proton và neutron. Sự khác biệt về điện tích và khối lượng này tạo nên sự khác biệt trong vai trò của chúng trong cấu tạo nguyên tử.
Điện tích và số lượng hạt
Điện tích nguyên tử
Trong một nguyên tử trung hòa về điện, số lượng proton (điện tích dương) bằng số lượng electron (điện tích âm). Do đó, tổng điện tích của nguyên tử bằng 0. Nếu nguyên tử mất hoặc nhận thêm electron, nó sẽ trở thành ion, mang điện tích dương (ion dương) hoặc âm (ion âm).
Số khối và số hiệu nguyên tử
Số khối của một nguyên tử là tổng số proton và neutron trong hạt nhân. Số hiệu nguyên tử bằng số lượng proton (cũng bằng số lượng electron trong nguyên tử trung hòa). Hai đại lượng này giúp xác định đặc điểm của mỗi nguyên tố hóa học.
Sản phẩm hữu ích: vẽ vạn lý trường thành đơn giản
Xem thêm: một triệu năm trăm nghìn đồng, viết bằng số
Sản phẩm liên quan: cơ năng của vật m là 375j
Xem thêm: số đơn vị điện tích hạt nhân nguyên tử kí hiệu là z của một nguyên tố gọi là