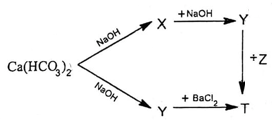
Phản ứng Ca(HCO3)2 + NaOH tỉ lệ 1:1
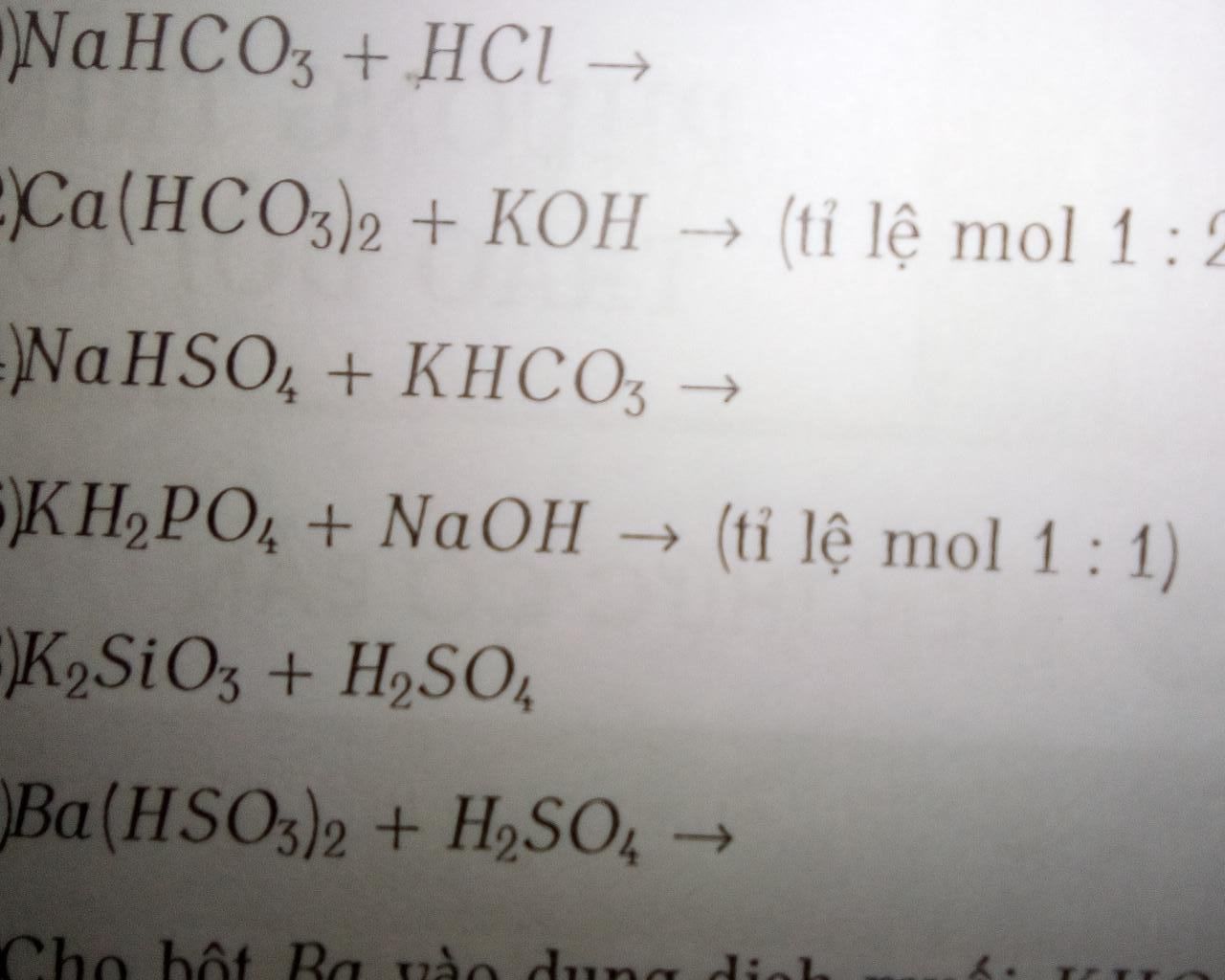
Chính Sách Vận Chuyển Và Đổi Trả Hàng
Miễn phí vận chuyển mọi đơn hàng từ 500K
- Phí ship mặc trong nước 50K
- Thời gian nhận hàng 2-3 ngày trong tuần
- Giao hàng hỏa tốc trong 24h
- Hoàn trả hàng trong 30 ngày nếu không hài lòng
Mô tả sản phẩm
Phản ứng giữa Ca(HCO3)2 và NaOH với tỉ lệ mol 1:1 tạo ra kết tủa CaCO3 và dung dịch NaHCO3. Phương trình phản ứng như sau: Ca(HCO3)2 + 2NaOH → CaCO3↓ + 2NaHCO3 + H2O. Tuy nhiên, nếu tỉ lệ mol không chính xác là 1:1, sản phẩm thu được sẽ khác.
Chi tiết phản ứng Ca(HCO3)2 + NaOH tỉ lệ 1:1
Phương trình phản ứng và giải thích
Phương trình ion rút gọn của phản ứng là: Ca2+ + 2HCO3- + 2Na+ + 2OH- → CaCO3↓ + 2Na+ + 2H2O + CO32-. Như bạn thấy, ion Ca2+ kết hợp với ion CO32- tạo thành kết tủa trắng CaCO3 không tan trong nước. Ion HCO3- phản ứng với ion OH- tạo thành ion CO32- và nước. Đây là phản ứng trung hòa một phần. Việc tạo thành kết tủa CaCO3 là điểm quan trọng của phản ứng này.Điều kiện phản ứng
Phản ứng xảy ra ở điều kiện thường, không cần đun nóng. Tuy nhiên, tốc độ phản ứng có thể bị ảnh hưởng bởi nhiệt độ và nồng độ của các chất tham gia.Ứng dụng
Phản ứng này có ứng dụng trong việc xác định nồng độ của Ca(HCO3)2 hoặc NaOH bằng phương pháp chuẩn độ. Nó cũng được ứng dụng trong một số quá trình xử lý nước thải, nhằm loại bỏ ion canxi.Lưu ý
Nếu tỉ lệ mol giữa Ca(HCO3)2 và NaOH không phải là 1:1, sản phẩm thu được sẽ khác. Ví dụ, nếu NaOH dư, toàn bộ Ca(HCO3)2 sẽ phản ứng tạo thành CaCO3 và NaHCO3. Ngược lại, nếu Ca(HCO3)2 dư, chỉ một phần Ca(HCO3)2 sẽ phản ứng, phần còn lại sẽ không phản ứng. Việc kiểm soát chính xác tỉ lệ mol là rất quan trọng để đảm bảo sản phẩm mong muốn.Xem thêm: bài thơ chiều tối được sáng tác trong hoàn cảnh nào
Xem thêm: come up against là gì
Xem thêm: bring sth up là gì
Sản phẩm hữu ích: biện pháp tương phản
Sản phẩm hữu ích: đề ôn luyện toán lớp 3