Cách Điều Chế H2SO4
Chính Sách Vận Chuyển Và Đổi Trả Hàng
Miễn phí vận chuyển mọi đơn hàng từ 500K
- Phí ship mặc trong nước 50K
- Thời gian nhận hàng 2-3 ngày trong tuần
- Giao hàng hỏa tốc trong 24h
- Hoàn trả hàng trong 30 ngày nếu không hài lòng
Mô tả sản phẩm
Axit sunfuric (H2SO4) được điều chế chủ yếu bằng hai phương pháp chính: phương pháp tiếp xúc và phương pháp thủy phân. Phương pháp tiếp xúc là phương pháp công nghiệp phổ biến nhất để sản xuất H2SO4 với quy mô lớn, cho chất lượng cao và hiệu suất tốt. Còn phương pháp thủy phân thường được sử dụng trong phòng thí nghiệm với quy mô nhỏ hơn.
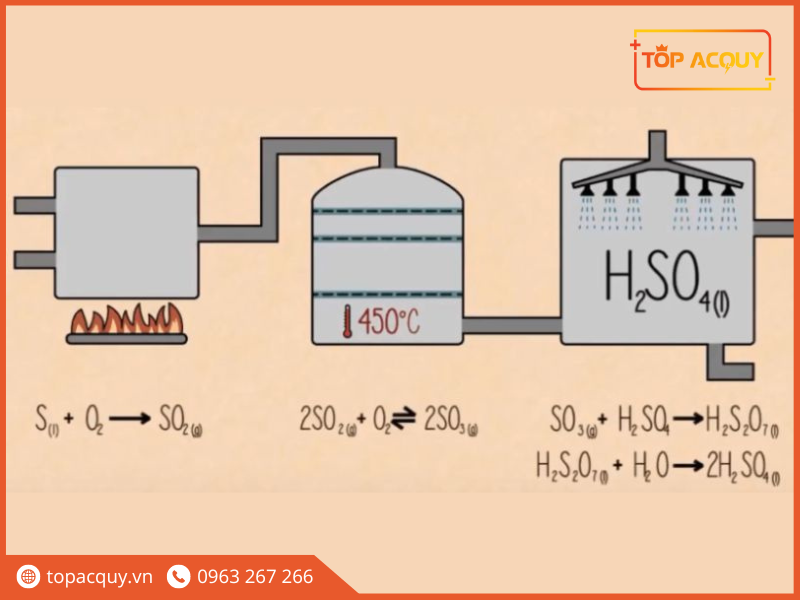
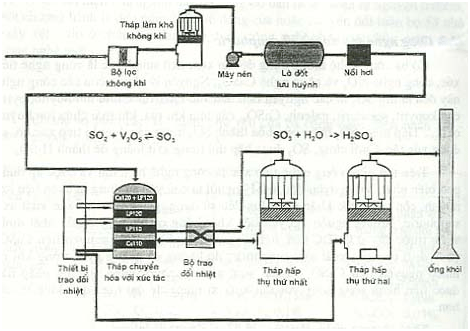
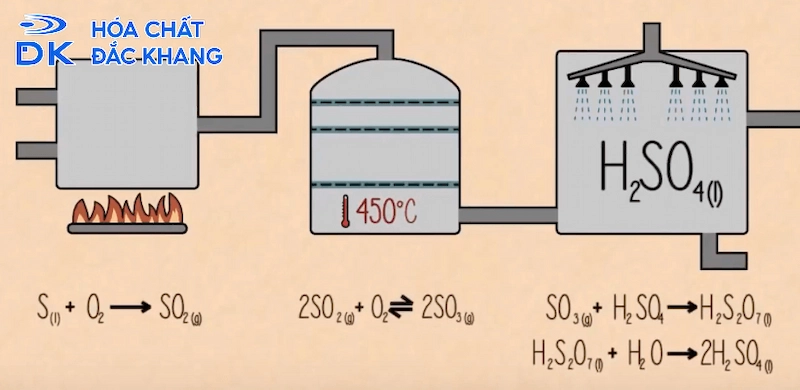
Phương pháp tiếp xúc
Các giai đoạn chính:
- Sản xuất SO2: Đốt cháy lưu huỳnh hoặc quặng pirit (FeS2) trong không khí.
- Oxi hóa SO2 thành SO3: SO2 được oxi hóa thành SO3 bằng xúc tác V2O5 ở nhiệt độ khoảng 450-500°C. Đây là giai đoạn quan trọng nhất, cần kiểm soát chặt chẽ nhiệt độ và nồng độ để đạt hiệu suất cao.
- Hấp thụ SO3: SO3 được hấp thụ vào H2SO4 98% để tạo thành oleum (H2S2O7). Oleum sau đó được pha loãng bằng nước để thu được H2SO4 có nồng độ mong muốn.
Phương pháp tiếp xúc cho phép sản xuất H2SO4 với độ tinh khiết cao và hiệu suất lớn, đáp ứng nhu cầu công nghiệp.
Phương pháp thủy phân
Quá trình điều chế:
Phương pháp này thường sử dụng phản ứng giữa SO3 với nước: SO3 + H2O → H2SO4. Tuy nhiên, phản ứng này xảy ra rất mãnh liệt và tạo ra nhiều nhiệt, dẫn đến hiện tượng tạo thành sương mù axit khó thu hồi. Do đó, trong thực tế, người ta thường hấp thụ SO3 vào H2SO4 đậm đặc để tạo thành oleum, sau đó pha loãng oleum bằng nước để thu được H2SO4.
Phương pháp thủy phân ít được sử dụng trong công nghiệp do hiệu suất thấp và khó kiểm soát.
Tóm lại, việc lựa chọn phương pháp điều chế H2SO4 phụ thuộc vào quy mô sản xuất, chất lượng sản phẩm yêu cầu và các yếu tố kinh tế.
Sản phẩm liên quan: tính điện thế tại một điểm
Sản phẩm hữu ích: tầm trung là gì
Sản phẩm hữu ích: đường kính của hình tròn là gì