Nhóm Nguyên Tố Hóa Học: Phân Loại và Tính Chất
Chính Sách Vận Chuyển Và Đổi Trả Hàng
Miễn phí vận chuyển mọi đơn hàng từ 500K
- Phí ship mặc trong nước 50K
- Thời gian nhận hàng 2-3 ngày trong tuần
- Giao hàng hỏa tốc trong 24h
- Hoàn trả hàng trong 30 ngày nếu không hài lòng
Mô tả sản phẩm
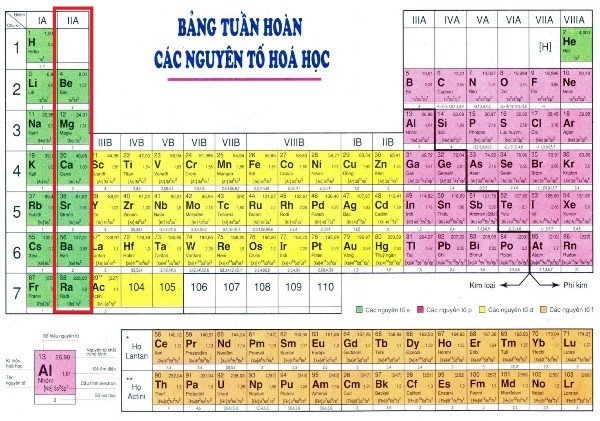
Các nhóm nguyên tố hóa học là cách phân loại các nguyên tố dựa trên cấu hình electron lớp ngoài cùng, dẫn đến sự tương đồng về tính chất hóa học. Việc hiểu rõ về các nhóm nguyên tố giúp chúng ta dự đoán và lý giải các phản ứng hóa học một cách hiệu quả hơn. Bài viết này sẽ cung cấp thông tin chi tiết về các nhóm nguyên tố quan trọng.
Nhóm nguyên tố kim loại kiềm (Nhóm IA)
Tính chất đặc trưng:
Các nguyên tố nhóm IA (Li, Na, K, Rb, Cs, Fr) có 1 electron ở lớp ngoài cùng, dễ dàng nhường electron để tạo thành ion dương 1+. Chúng rất hoạt động hóa học, phản ứng mạnh với nước tạo ra hydro và bazơ. Chúng có điểm nóng chảy và điểm sôi thấp.
Nhóm nguyên tố kim loại kiềm thổ (Nhóm IIA)
Tính chất đặc trưng:
Các nguyên tố nhóm IIA (Be, Mg, Ca, Sr, Ba, Ra) có 2 electron ở lớp ngoài cùng, dễ nhường 2 electron để tạo thành ion dương 2+. Chúng cũng là kim loại hoạt động hóa học, nhưng kém hoạt động hơn nhóm IA. Chúng có điểm nóng chảy và điểm sôi cao hơn nhóm IA.
Nhóm nguyên tố halogen (Nhóm VIIA)
Tính chất đặc trưng:
Các nguyên tố nhóm VIIA (F, Cl, Br, I, At) có 7 electron ở lớp ngoài cùng, dễ dàng nhận thêm 1 electron để tạo thành ion âm 1-. Chúng là các phi kim rất hoạt động hóa học, phản ứng mạnh với nhiều kim loại và phi kim khác. Tính oxi hóa giảm dần từ F đến At.
Nhóm nguyên tố khí hiếm (Nhóm VIIIA)
Tính chất đặc trưng:
Các nguyên tố nhóm VIIIA (He, Ne, Ar, Kr, Xe, Rn) có lớp electron ngoài cùng bão hòa (8 electron, trừ He chỉ có 2 electron). Chúng rất trơ về mặt hóa học, ít tham gia phản ứng hóa học do cấu hình electron bền vững.
Nhóm nguyên tố chuyển tiếp
Tính chất đặc trưng:
Các nguyên tố chuyển tiếp nằm ở giữa bảng tuần hoàn. Chúng có electron ở cả lớp ngoài cùng và lớp sát ngoài cùng, dẫn đến tính chất hóa học đa dạng và phức tạp hơn các nhóm nguyên tố khác. Chúng thường tạo ra nhiều trạng thái oxi hóa khác nhau và tạo thành các hợp chất có màu sắc đặc trưng.
Sản phẩm hữu ích: công thức hình học toán 12
Xem thêm: trâu trắng có ý nghĩa gì
Xem thêm: day hoat dong hoa hoc
Sản phẩm hữu ích: vẽ lọ hoa sen
Sản phẩm hữu ích: công thức cấu tạo ch3cooh