Các Loại Liên Kết Hóa Học
Chính Sách Vận Chuyển Và Đổi Trả Hàng
Miễn phí vận chuyển mọi đơn hàng từ 500K
- Phí ship mặc trong nước 50K
- Thời gian nhận hàng 2-3 ngày trong tuần
- Giao hàng hỏa tốc trong 24h
- Hoàn trả hàng trong 30 ngày nếu không hài lòng
Mô tả sản phẩm
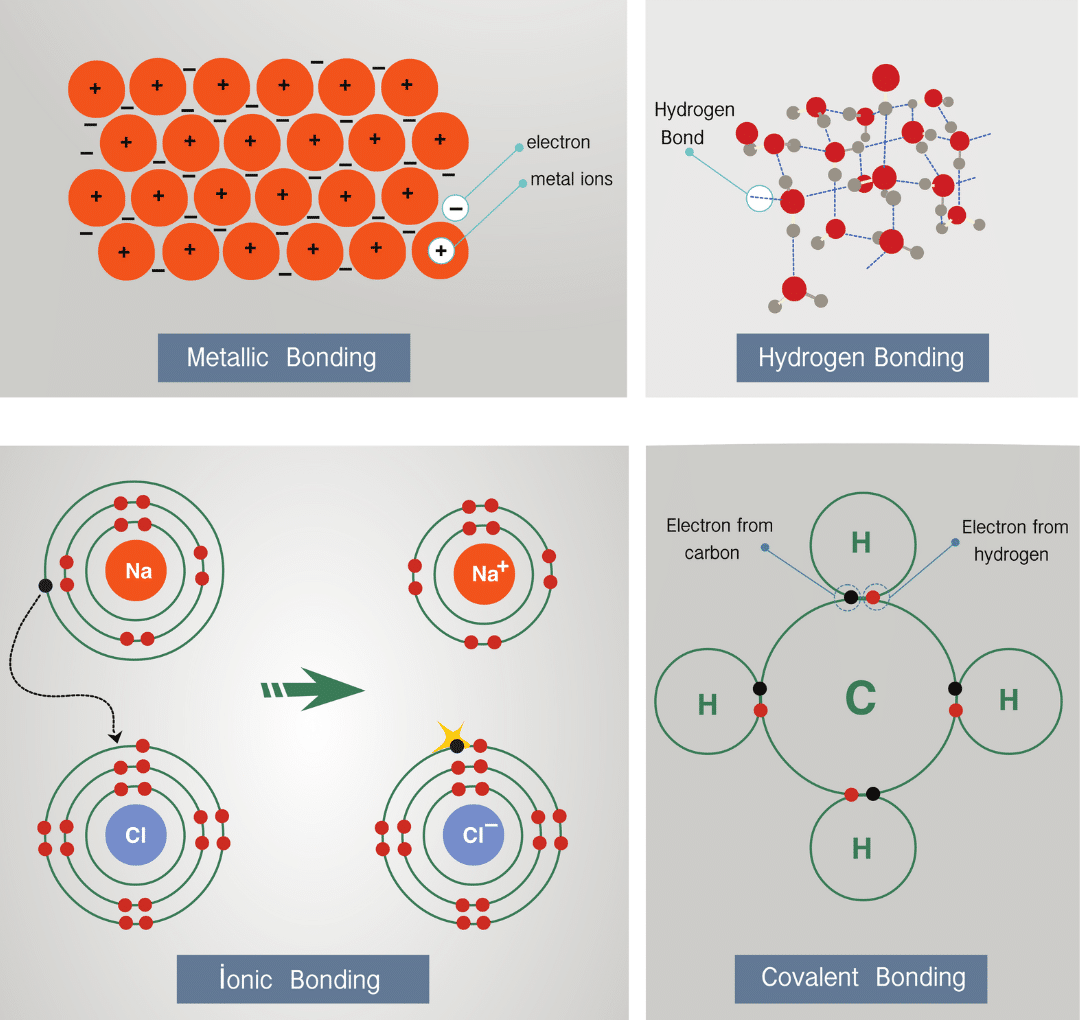
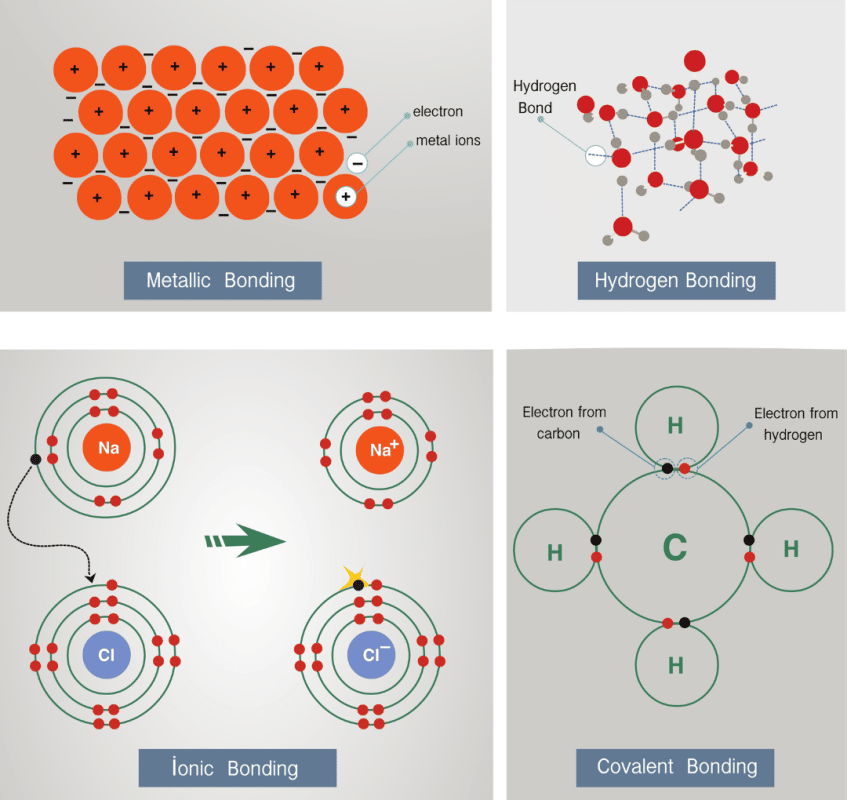
Có ba loại liên kết hóa học chính: liên kết ion, liên kết cộng hóa trị và liên kết kim loại. Mỗi loại liên kết được hình thành bằng cách chia sẻ hoặc chuyển giao electron giữa các nguyên tử, tạo ra sự ổn định về mặt năng lượng. Sự khác biệt giữa chúng nằm ở cách electron được chia sẻ hoặc chuyển giao.
Liên Kết Ion
Đặc điểm của Liên Kết Ion
Liên kết ion hình thành giữa các nguyên tử có độ âm điện chênh lệch lớn. Nguyên tử kim loại (có độ âm điện thấp) sẽ nhường electron cho nguyên tử phi kim (có độ âm điện cao), tạo ra các ion mang điện tích trái dấu. Lực hút tĩnh điện giữa các ion dương và ion âm tạo nên liên kết ion. Ví dụ điển hình là liên kết giữa natri (Na) và clo (Cl) tạo thành muối ăn (NaCl). Các hợp chất ion thường có điểm nóng chảy và điểm sôi cao, dễ tan trong nước và dẫn điện khi nóng chảy hoặc hòa tan trong dung dịch.
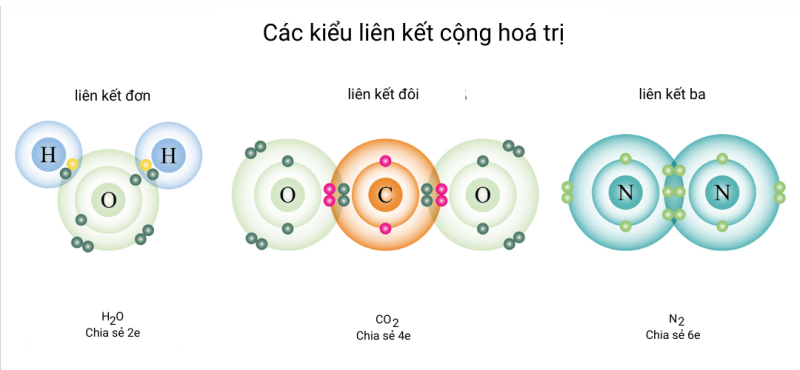
Liên Kết Cộng Hóa Trị
Đặc điểm của Liên Kết Cộng Hóa Trị
Liên kết cộng hóa trị hình thành khi các nguyên tử chia sẻ các electron với nhau. Loại liên kết này thường xảy ra giữa các nguyên tử phi kim có độ âm điện tương đương nhau. Mỗi nguyên tử góp electron vào liên kết để đạt được cấu hình electron bền vững. Có hai loại liên kết cộng hóa trị: liên kết cộng hóa trị không cực (khi độ âm điện của các nguyên tử bằng nhau) và liên kết cộng hóa trị cực (khi độ âm điện của các nguyên tử khác nhau). Ví dụ: liên kết trong phân tử khí hidro (H2) là liên kết cộng hóa trị không cực, trong khi liên kết trong phân tử nước (H2O) là liên kết cộng hóa trị cực.
Liên Kết Kim Loại
Đặc điểm của Liên Kết Kim Loại
Liên kết kim loại xảy ra giữa các nguyên tử kim loại. Trong liên kết này, các electron hóa trị di chuyển tự do giữa các nguyên tử kim loại, tạo thành "biển electron". Lực hút tĩnh điện giữa các ion dương kim loại và "biển electron" này giữ các nguyên tử kim loại lại với nhau. Các kim loại thường có tính dẫn điện và dẫn nhiệt tốt, dễ dát mỏng và kéo thành sợi.
Xem thêm: công thức tính thời gian rơi của vật
Sản phẩm liên quan: hiện tượng khúc xạ ánh sáng là hiện tượng ánh sáng bị
Sản phẩm hữu ích: thỏ con ăn gì
Xem thêm: bảng hệ thống tuần hoàn mới nhất
Sản phẩm liên quan: sản xuất cao su