Bazơ không tan là gì? Danh sách các bazơ không tan và tính chất
Chính Sách Vận Chuyển Và Đổi Trả Hàng
Miễn phí vận chuyển mọi đơn hàng từ 500K
- Phí ship mặc trong nước 50K
- Thời gian nhận hàng 2-3 ngày trong tuần
- Giao hàng hỏa tốc trong 24h
- Hoàn trả hàng trong 30 ngày nếu không hài lòng
Mô tả sản phẩm
Bazơ không tan là những hợp chất bazơ có độ tan trong nước rất thấp hoặc không tan. Chúng thường là các hidroxit của kim loại ít hoạt động. Việc hiểu rõ về các bazơ không tan rất quan trọng trong hóa học.
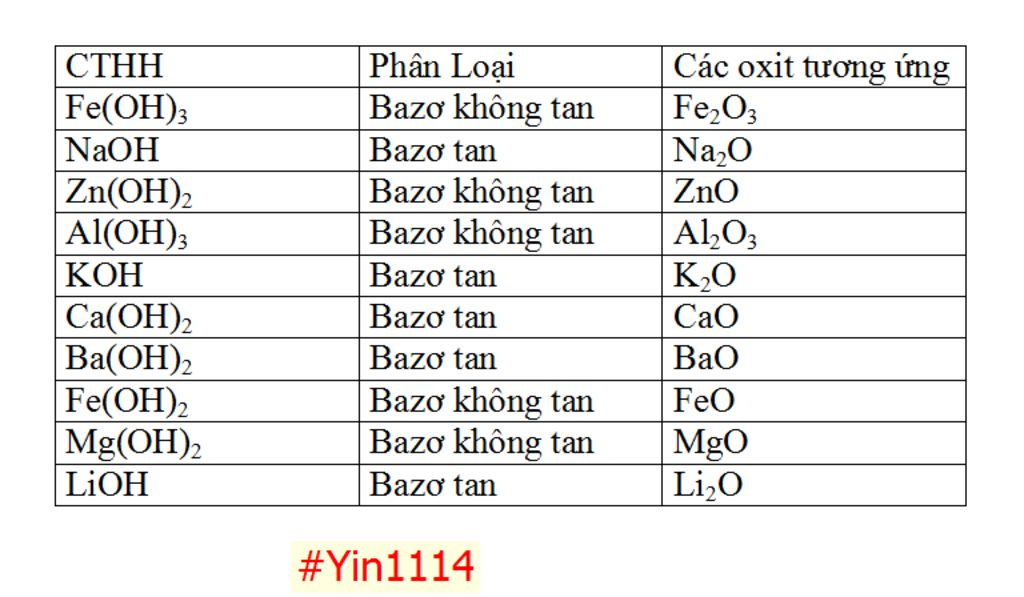
Danh sách một số bazơ không tan
Các bazơ không tan phổ biến:
- Cu(OH)2 (Đồng (II) hidroxit): Kết tủa màu xanh lam
- Fe(OH)3 (Sắt (III) hidroxit): Kết tủa màu nâu đỏ
- Fe(OH)2 (Sắt (II) hidroxit): Kết tủa màu trắng xanh, nhanh chóng chuyển sang màu nâu đỏ khi tiếp xúc với không khí
- Al(OH)3 (Nhôm hidroxit): Kết tủa màu trắng keo
- Zn(OH)2 (Kẽm hidroxit): Kết tủa màu trắng
- Cr(OH)3 (Crom (III) hidroxit): Kết tủa màu lục xám
- Mg(OH)2 (Magie hidroxit): Kết tủa màu trắng, ít tan hơn các bazơ khác trong danh sách này.
- Pb(OH)2 (Chì (II) hidroxit): Kết tủa màu trắng
Lưu ý:
Độ tan của bazơ có thể phụ thuộc vào nhiều yếu tố như nhiệt độ, pH của dung dịch. Một số bazơ được coi là không tan thực tế vẫn có một lượng rất nhỏ tan trong nước.Tính chất của bazơ không tan
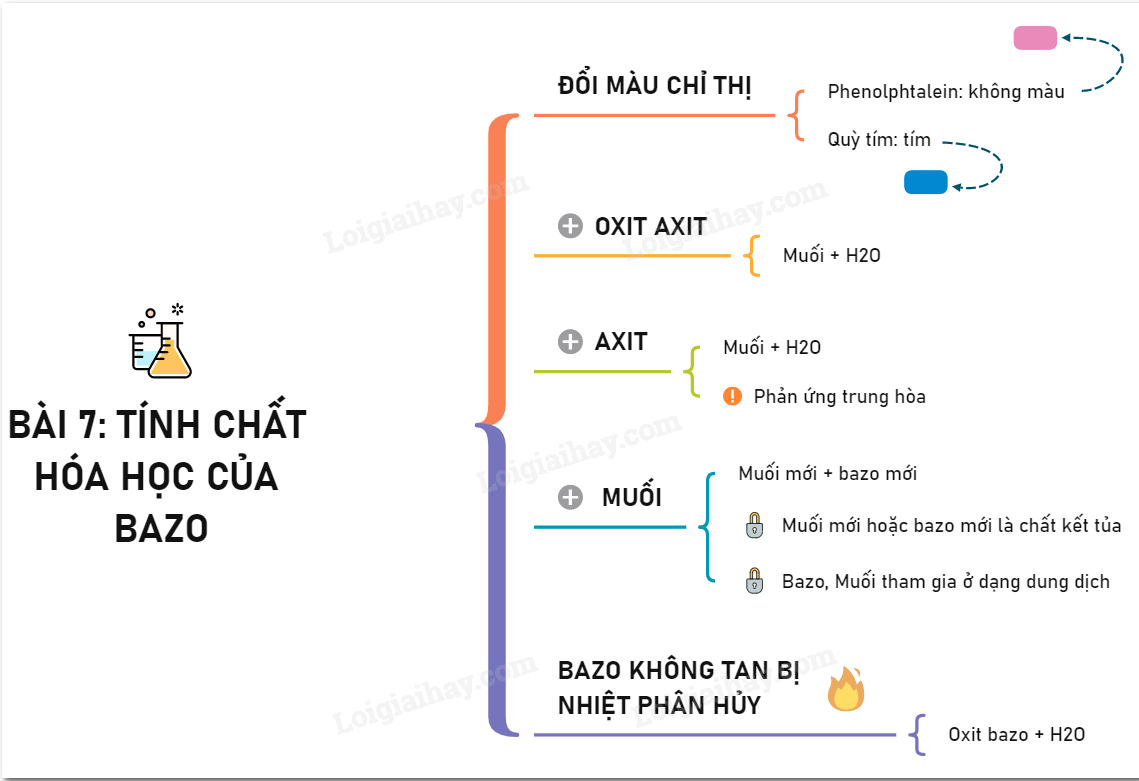
Bazơ không tan thường có những tính chất sau:
- Không làm đổi màu quỳ tím khi ở dạng rắn.
- Phản ứng với axit tạo thành muối và nước (phản ứng trung hòa).
- Một số bazơ không tan bị nhiệt phân hủy tạo thành oxit kim loại và nước.
- Thường xuất hiện dưới dạng kết tủa khi phản ứng xảy ra trong dung dịch.
- Màu sắc đa dạng, giúp nhận biết một số chất.
Hiểu rõ về tính chất và danh sách các bazơ không tan giúp chúng ta giải quyết nhiều bài toán hóa học, đặc biệt là trong các phản ứng tạo kết tủa, nhận biết chất và cân bằng phương trình hóa học.
Xem thêm: công dụng của nguồn điện
Sản phẩm hữu ích: đề thi lớp 3 kì 1
Sản phẩm hữu ích: c 6 h 12 oh 6 + agno3
Xem thêm: bài tập toán lớp 4 kết nối tri thức