Axit mạnh và yếu: Sự khác biệt và phân loại

Chính Sách Vận Chuyển Và Đổi Trả Hàng
Miễn phí vận chuyển mọi đơn hàng từ 500K
- Phí ship mặc trong nước 50K
- Thời gian nhận hàng 2-3 ngày trong tuần
- Giao hàng hỏa tốc trong 24h
- Hoàn trả hàng trong 30 ngày nếu không hài lòng
Mô tả sản phẩm
Axit mạnh là những axit phân ly hoàn toàn trong dung dịch nước, tạo ra nồng độ ion H+ cao. Ngược lại, axit yếu chỉ phân ly một phần, tạo ra nồng độ ion H+ thấp hơn. Sự khác biệt này ảnh hưởng đến độ pH và tính chất hóa học của dung dịch.
Phân loại axit mạnh và yếu
Axit mạnh
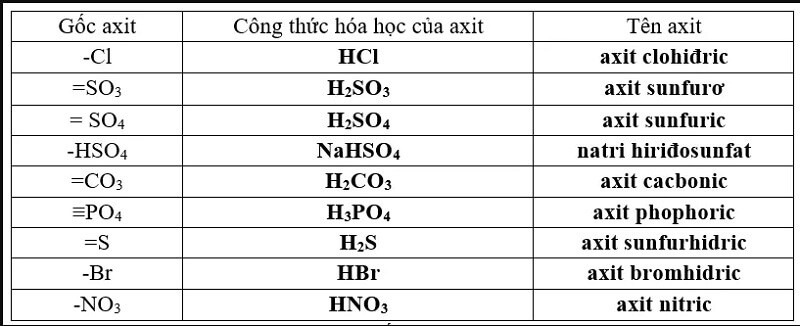
Các axit mạnh thường gặp bao gồm: HCl (axit clohydric), HBr (axit bromhydric), HI (axit iodhydric), HNO3 (axit nitric), H2SO4 (axit sunfuric) và HClO4 (axit pecloric). Chúng phân ly hoàn toàn trong nước, nghĩa là gần như tất cả các phân tử axit đều tạo thành ion H+ và anion tương ứng. Điều này dẫn đến độ pH rất thấp của dung dịch.
Axit yếu
Axit yếu chỉ phân ly một phần trong nước. Một số ví dụ về axit yếu bao gồm: CH3COOH (axit axetic), H2CO3 (axit cacbonic), H3PO4 (axit photphoric), HF (axit flohydric) và nhiều axit hữu cơ khác. Sự phân ly không hoàn toàn này dẫn đến nồng độ ion H+ thấp hơn so với axit mạnh cùng nồng độ, do đó pH của dung dịch axit yếu cao hơn.
Sự khác biệt về độ mạnh
Sự khác biệt giữa axit mạnh và yếu được thể hiện rõ nhất qua hằng số phân ly axit (Ka). Axit mạnh có Ka rất lớn (thường lớn hơn 1), trong khi axit yếu có Ka nhỏ (thường nhỏ hơn 1). Ka càng lớn, axit càng mạnh và càng dễ phân ly thành ion H+.
Ứng dụng của axit mạnh và yếu
Cả axit mạnh và yếu đều có nhiều ứng dụng quan trọng trong công nghiệp và đời sống. Axit mạnh thường được sử dụng trong sản xuất các chất tẩy rửa, pin, và trong một số phản ứng hóa học đặc biệt. Axit yếu được sử dụng rộng rãi trong thực phẩm, dược phẩm và mỹ phẩm do tính chất ít gây ăn mòn hơn.
Tổng kết
Hiểu rõ sự khác biệt giữa axit mạnh và yếu là rất quan trọng trong hóa học. Sự khác biệt này ảnh hưởng đến tính chất hóa học, độ pH và ứng dụng của các axit này.
Xem thêm: ac si met
Sản phẩm liên quan: bầu uống hoa đậu biếc được không
Sản phẩm hữu ích: de thi giữa kì 2 lớp 3 môn tiếng việt có đáp án