Al + HNO3 → N2O: Phản ứng và Điều kiện phản ứng

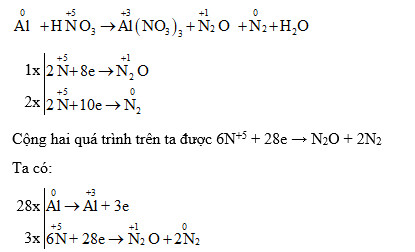

Chính Sách Vận Chuyển Và Đổi Trả Hàng
Miễn phí vận chuyển mọi đơn hàng từ 500K
- Phí ship mặc trong nước 50K
- Thời gian nhận hàng 2-3 ngày trong tuần
- Giao hàng hỏa tốc trong 24h
- Hoàn trả hàng trong 30 ngày nếu không hài lòng
Mô tả sản phẩm
Phản ứng giữa nhôm (Al) và axit nitric (HNO3) tạo ra khí N2O là một phản ứng oxi hóa khử phức tạp, phụ thuộc rất nhiều vào nồng độ của HNO3 và nhiệt độ phản ứng. Không phải lúc nào phản ứng cũng tạo ra N2O, mà còn có thể tạo ra các sản phẩm khử nitơ khác như NO, NO2 hoặc NH4NO3.
Điều kiện để Al + HNO3 tạo ra N2O
Nồng độ HNO3:
Nồng độ HNO3 ảnh hưởng quyết định đến sản phẩm tạo thành. Để tạo ra N2O, cần sử dụng HNO3 loãng và lạnh. Nếu HNO3 đặc hoặc nóng, các sản phẩm khử khác sẽ được ưu tiên tạo thành.Nhiệt độ:
Phản ứng cần được thực hiện ở nhiệt độ thấp. Nhiệt độ cao sẽ làm tăng khả năng tạo ra các sản phẩm khử khác thay vì N2O.Tỉ lệ mol:
Tỉ lệ mol giữa Al và HNO3 cũng cần được cân nhắc để tối ưu hóa quá trình tạo N2O. Thực tế, điều này cần được xác định thông qua thí nghiệm cụ thể.Phương trình phản ứng cân bằng
Việc viết phương trình phản ứng cân bằng cho phản ứng Al + HNO3 → N2O khá phức tạp do nó phụ thuộc vào nhiều yếu tố. Không có một phương trình duy nhất áp dụng cho mọi điều kiện. Tuy nhiên, một phương trình minh họa có thể là: ( cần cân bằng tùy thuộc vào điều kiện thực tế) 8Al + 30HNO3 → 8Al(NO3)3 + 3N2O + 15H2OỨng dụng và tầm quan trọng
Hiểu rõ phản ứng Al + HNO3 → N2O rất quan trọng trong nhiều lĩnh vực, bao gồm: Nghiên cứu hóa học, tổng hợp hóa chất, và các ứng dụng công nghiệp liên quan đến nhôm và axit nitric.Sản phẩm liên quan: alcl3 + nh3 + h2o pt ion
Sản phẩm hữu ích: lời bài hát ru lại câu hò
Xem thêm: like my father hợp âm
Sản phẩm liên quan: sự tích sông hồ ở tây nguyên