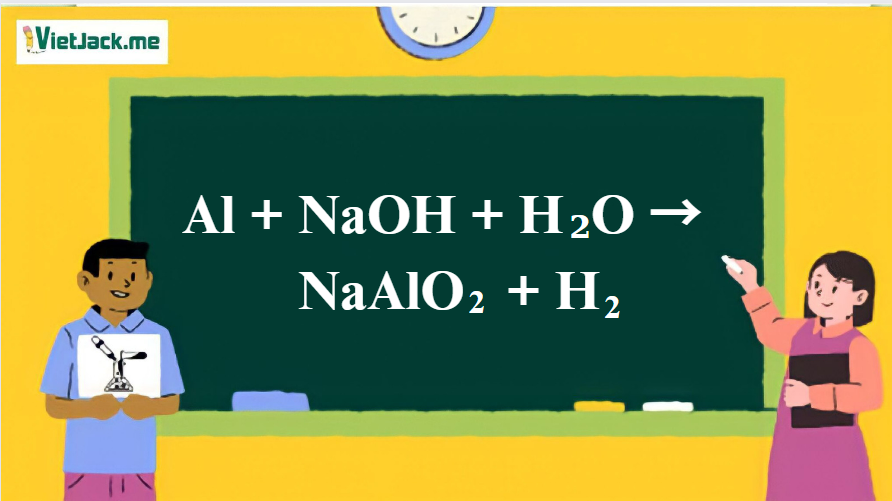
Phản ứng Al + H2O + NaOH: Giải thích chi tiết

Chính Sách Vận Chuyển Và Đổi Trả Hàng
Miễn phí vận chuyển mọi đơn hàng từ 500K
- Phí ship mặc trong nước 50K
- Thời gian nhận hàng 2-3 ngày trong tuần
- Giao hàng hỏa tốc trong 24h
- Hoàn trả hàng trong 30 ngày nếu không hài lòng
Mô tả sản phẩm
Phản ứng của nhôm (Al) với nước (H₂O) và natri hydroxit (NaOH) tạo ra muối natri aluminat (NaAlO₂) và khí hydro (H₂). Đây là phản ứng tỏa nhiệt và cần điều kiện nhất định để xảy ra.
Cơ chế phản ứng Al + H2O + NaOH
Sự hòa tan của Al trong dung dịch NaOH
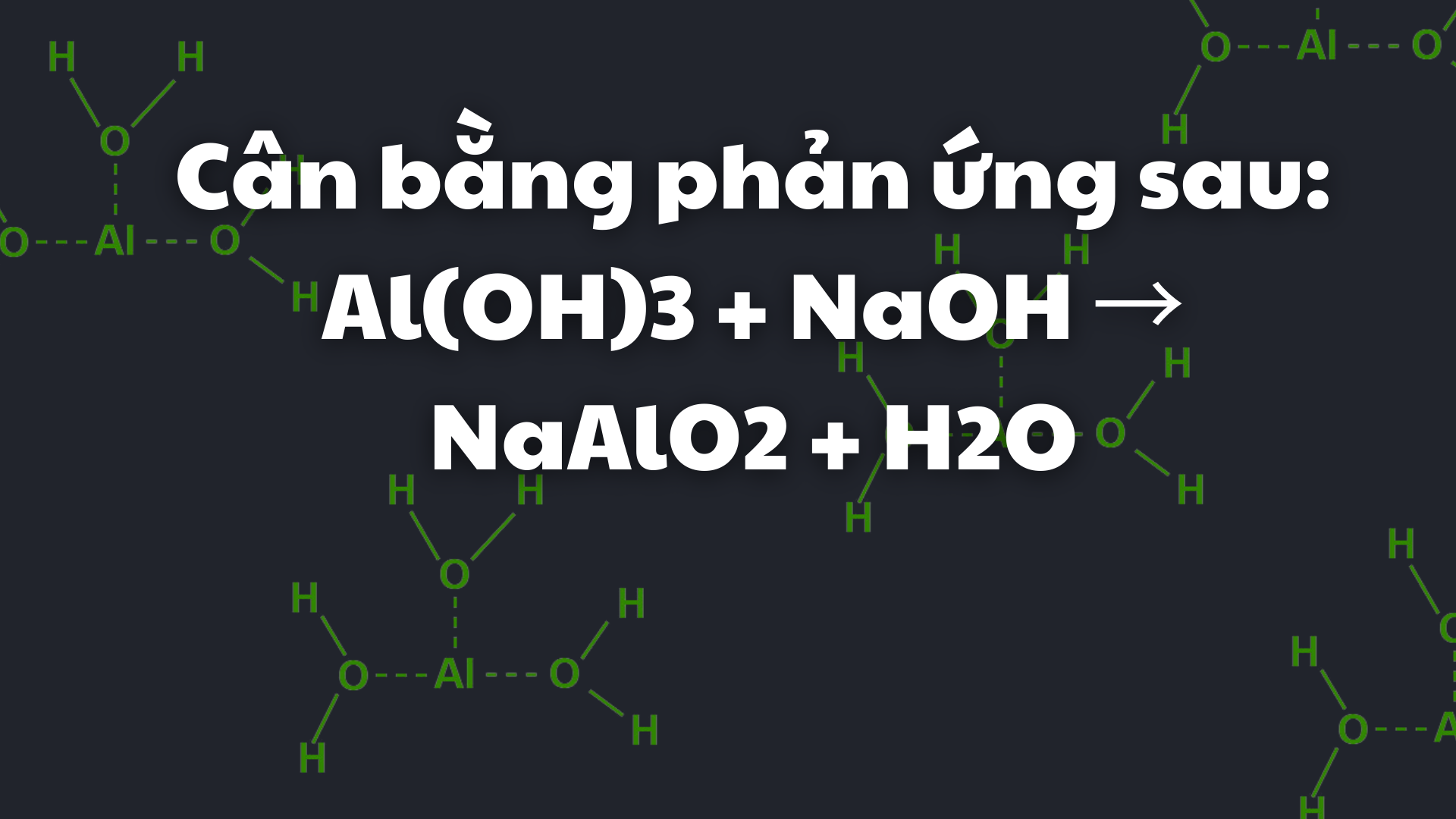
Nhôm là kim loại lưỡng tính, có thể phản ứng với cả axit và bazơ mạnh. Trong dung dịch NaOH, nhôm phản ứng tạo thành ion aluminat [Al(OH)₄]⁻, sau đó phân ly thành NaAlO₂. Quá trình này tạo điều kiện cho phản ứng tiếp tục diễn ra.Phản ứng của Al với nước
Mặc dù nhôm phản ứng chậm với nước ở nhiệt độ thường do lớp màng oxit Al₂O₃ bảo vệ bề mặt, nhưng sự có mặt của NaOH phá vỡ lớp màng này, cho phép nhôm tiếp xúc trực tiếp với nước. Nước phân ly thành ion H⁺ và OH⁻, nhưng phản ứng chính xảy ra là giữa Al và ion OH⁻.Tổng quan phản ứng
Phương trình phản ứng cân bằng: 2Al + 2NaOH + 6H₂O → 2Na[Al(OH)₄] + 3H₂Điều kiện phản ứng
Phản ứng xảy ra hiệu quả hơn ở nhiệt độ cao và khi có sự khuấy trộn. Lớp màng oxit Al₂O₃ trên bề mặt nhôm cần được loại bỏ hoặc làm yếu đi để phản ứng xảy ra nhanh chóng.Ứng dụng
Phản ứng này được ứng dụng trong công nghiệp sản xuất nhôm, tinh chế nhôm, và một số quá trình hóa học khác.Lưu ý an toàn
Phản ứng này giải phóng khí hydro dễ cháy, vì vậy cần thực hiện trong môi trường thông thoáng và tránh lửa. NaOH là chất ăn mòn mạnh, cần sử dụng đồ bảo hộ cá nhân khi thực hiện thí nghiệm.Sản phẩm hữu ích: nằm mơ thấy thỏ trắng
Sản phẩm liên quan: quy khư là gì
Xem thêm: ag + h2so4 đặc nguội